本文來自格隆匯專欄:平安醫藥葉寅,作者:葉寅 黃施齊
摘要
ADC藥物展現臨牀治療潛力。ADC是由抗體、毒素和連接子組成的創新藥物,可以精準將毒素遞送至腫瘤細胞,從而發揮殺傷作用,被稱爲生物導彈。作爲集合體,ADC藥物結合了化療和精準療法的優點:相比化療具有更強的特異性、更小的副作用;相比抗體具備更強的腫瘤殺傷效果和旁觀者效應。全球目前已有12款上市的ADC藥物,治療領域主要集中在腫瘤方面,並且主要是用於患者的後線治療,包括復發/難治性和轉移性腫瘤。從療效數據來看,有多款ADC藥物的ORR或mPFS相比化療增長了約一倍,爲後線患者帶了更多的治療選擇和延長生存期的希望,進一步驗證了ADC藥物填補空白適應症以及取代傳統療法的治療潛力。
行業逐步迎來收穫期,市場潛力巨大。目前已上市的3款第三代ADC藥物Polivy、Enhertu和Padcev在2020年均實現快速放量,分別實現收入1.69、3.91和2.22億美元,同比增長231%、211%和111100%,有望成爲全球重磅產品,體現了ADC藥物的市場潛力。根據Nature預測,2020年以前上市的10款ADC藥物到2026年其銷售總額將超過164億美元,未來幾年仍有較大發展空間。目前多數ADC藥物還處在臨牀階段,伴隨藥物研發推進,未來幾年ADC行業即將迎來收穫期,步入全面商業化時代,市場容量將持續擴大,賽道有望保持較高景氣度。
創新2.0時代關注ADC這類高壁壘賽道。從我國創新藥研發階段來看,過去爲了快速跟進國外成熟藥物的me-too類賽道同質性問題顯著,導致新藥上市可能就將面臨集採,陷入價格、銷售能力的比拼。伴隨研發能力提升,目前我國部分企業的研發正在逐步從創新1.0轉型到2.0階段,演變成差異化競爭,逐漸與國際接軌。在創新2.0時代我們需要關注ADC這類有臨牀價值和差異化的高壁壘賽道。ADC研發的核心主要包括三要素和組合技術,每個部分都具有設計難點,賽道護城河較寬,競爭格局良好。
投資建議:ADC藥物已在臨牀上展現顯著治療潛力,市場具有較大發展空間,在賽道中我們建議關注以下幾類企業:1)具備自主ADC技術平臺的企業。ADC作爲組合藥物,每一個組成部分都可以變化替換,具備自主技術平臺的企業能夠組合迭代不同產品,賦能產品管線研發,具有一定稀缺屬性;2)關注成熟靶點中進度靠前的企業,以及同靶點中分子設計升級的產品。由於我國ADC行業正在逐步從fast- follow轉型,因此目前處於臨牀後期的部分產品存在同質性問題,進度靠前的企業有望在上市後迅速佈局市場,先發優勢顯著,而差異性的分子設計有望提高藥物效果,搶佔市場。3)具備ADC藥物研發能力的CXO企業。ADC藥物開發門檻較高,部分企業爲了轉型附加值更高的ADC領域,將和具備研發能力的CRO企業合作,利好其業績表現。
01
不斷迭代升級的生物導彈藥物
1.1 ADC結合了化療和精準療法的優點
腫瘤治療領域的生物導彈。抗體偶聯藥物(Antibody–Drug Conjugates,ADC)是通過連接子將具有細胞毒活性的藥物(有效載荷)偶聯至抗體藥物組合而成的“生物導彈”。ADC藥物在進入血液後,其抗體部分將識別並結合靶細胞的表面抗原。在通過內吞作用將ADC-抗原複合物內化進細胞後,該複合物將被溶酶體降解,有效載荷被釋放出來,從而破壞DNA或微管,或發揮拓撲異構酶/RNA聚合酶抑制作用,最終導致細胞死亡,具有精準、殺傷力大的特性,是新一代治療藥物。
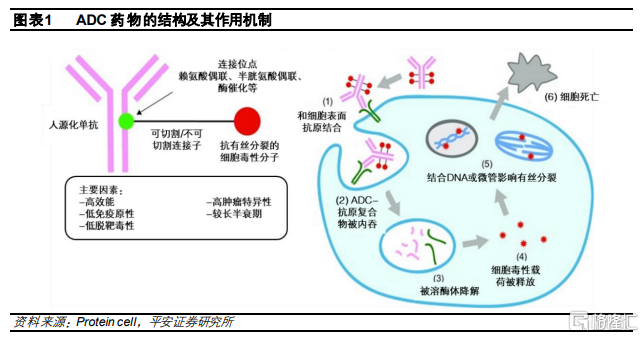
現有療法各有優缺點。過去腫瘤治療主要是以化療藥物爲主。化療是使用細胞毒藥物的首種系統性癌症治療方式,主要通過幹擾細胞週期,延緩或徹底阻止腫瘤細胞繁殖。但由於化療藥物也會對正常細胞進行無差別殺傷,因此會帶來嚴重的副作用。自2000年以來,以小分子靶向藥和抗體爲代表的精準療法的研發取得巨大進步,成爲腫瘤主要的治療方式。然而,由於小分子和抗體藥物主要是特異性靶向腫瘤信號通路或者腫瘤表面抗原,而腫瘤細胞間的異質性較強,並且可以通過調低抗原或使用補償通路實現逃逸,因此精準療法對於腫瘤的清除效率相比化療較爲有限。
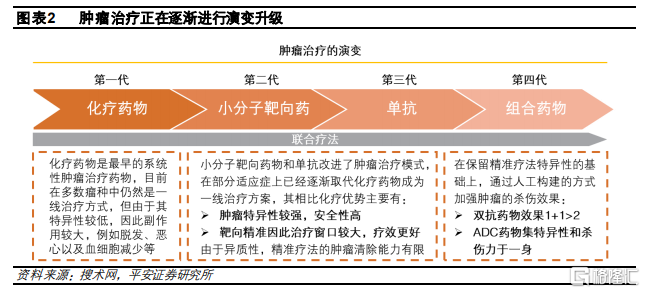
ADC結合了化療和精準治療的優勢。目前療法升級的主要趨勢是增強腫瘤殺傷的效力以降低最小有效劑量(MED),同時增加腫瘤選擇性以升高最大限制劑量(MTD),從而提高抗腫瘤藥物的治療指數。ADC作爲化療和抗體療法的結合體,有望能夠實現這個目標,增大化療藥物治療窗口,同時加強精準療法的殺傷力:ADC藥物的抗體部分實現了對於腫瘤的精準靶向,而細胞毒部分則進一步加強了腫瘤的殺傷能力,集化療藥物的殺傷力和精準療法的特異性於一身,並結合了小分子藥物和抗體藥物的特性,有望革新現有療法。

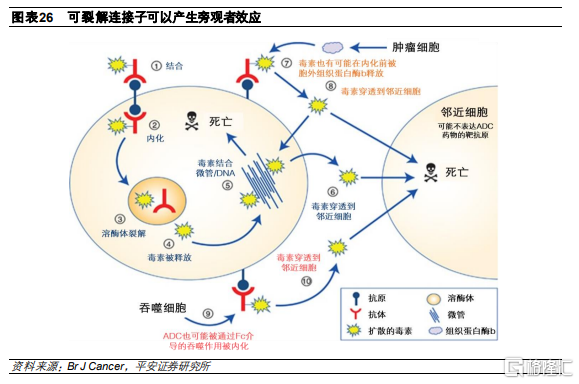
旁觀者效應助力解決腫瘤異質性問題。此外,ADC藥物可利用連接子的物理和化學特性,在被內化後可釋放出不帶電荷、可穿透細胞膜的有效載荷,從而殺傷臨近的抗原表達陰性的癌細胞。旁觀者殺傷效應對於抗原表達不均一的腫瘤細胞具有重要意義,進一步加強腫瘤清除效率。
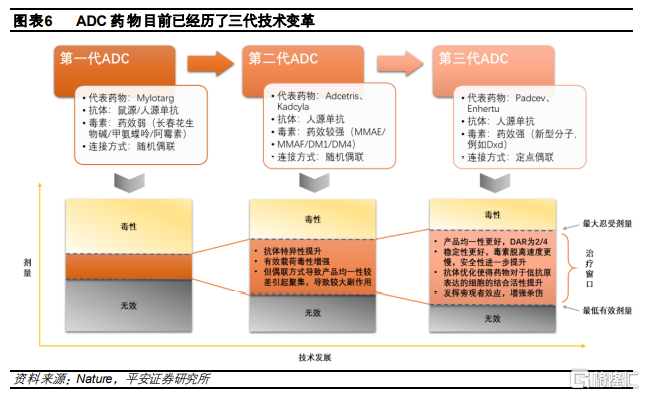
1.2 ADC藥物已歷經三代技術變革
ADC概念的提出最早可以追溯到100年以前,伴隨抗體技術和蛋白質重組工程的進步,越來越多的ADC藥物進入臨牀試驗甚至上市,從歷史來看,ADC藥物的發展主要分爲三個階段:
萌芽階段(1910-1980):免疫學之父Paul Ehrilich於1913年首次提出的“魔術子彈”的概念。基於這個概念,首款抗體-細胞毒偶聯藥物在1958年問世,但當時技術比較落後,並沒有成功。而伴隨1970年代雜交瘤技術的出現,基於單克隆抗體的全身治療問世,蛋白重組工程技術逐步成熟,ADC研發步入正式發展階段,出現首個進入動物試驗的ADC藥物。
摸索階段(1980-2000):雖然雜交瘤技術的出現推動抗體行業發展,但早期抗體主要以鼠源性爲主,存在較嚴重的免疫原性問題,使得早期ADC藥物的治療效果有限,臨牀成功率較低,存在顯著的副作用。直到1980年代,Greg Winter開創了人源化單克隆抗體的技術,ADC藥物的開發才取得了重大突破。然而,該技術仍然不成熟,首款ADC上市藥物Mylotarg於2000年獲批,但由於其在使用過程中出現致死性的肝毒性,因此於2010年退市。
成熟發展期(2000-至今):伴隨基礎研究和生物技術的持續發展,抗體的篩選壁壘大幅下降,同時,抗體發現、蛋白質工程、配方和遞送設備方面在這個時期都取得了巨大進步,這些進步繼續推動ADC藥物的發展:抗體靶標特異性和半衰期的提升,以及更高效小分子藥物的出現,共同驅動ADC技術的升級迭代。在這個階段大批ADC藥物獲批上市,行業進入收穫期。
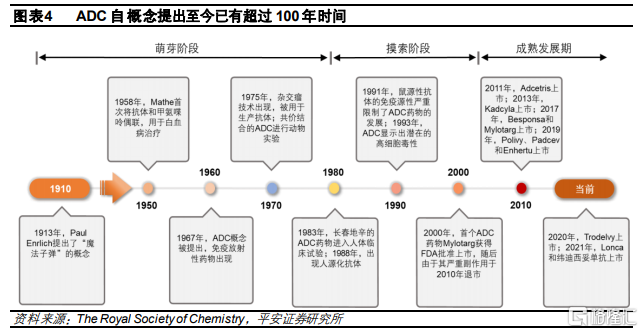
已上市ADC藥物展現相比現有療法更好的療效。歷經多年發展,全球目前已有12款上市的ADC藥物,治療領域主要集中在血液瘤和實體瘤方面,並且主要是用於患者的後線治療,包括晚期、復發/難治性以及轉移性的腫瘤適應症。從療效數據來看,ADC藥物給後線患者帶了更多的治療選擇和延長生存期的希望,有多款藥物的ORR或mPFS相比化療增長了約一倍,進一步驗證了ADC藥物取代傳統療法的治療潛力。
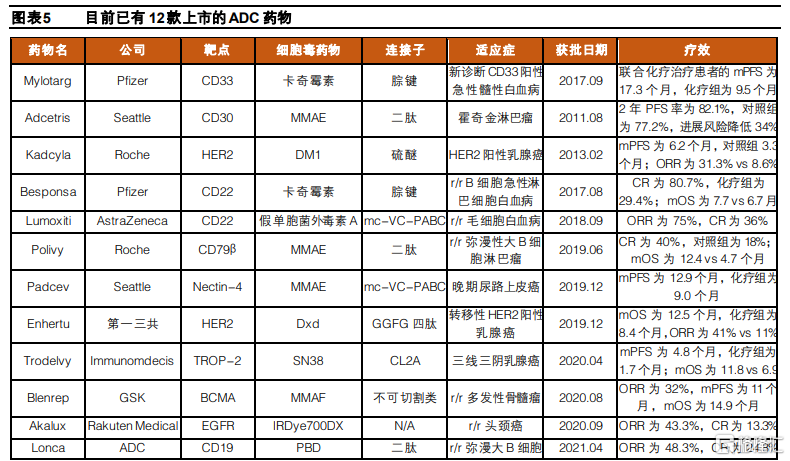

ADC藥物經過技術迭代持續拓展治療窗口。從藥物的構成和開發技術來看,已上市ADC藥物可以分爲三代。第一代ADC有效載荷毒性不夠強,且結構不夠穩定毒素較易脫落,導致治療窗口較小,大多以失敗告終。而伴隨抗體的發展,第二代ADC基本採用人源化單抗,並且使用更有效的細胞毒藥物,免疫原性的降低和藥效的提升使得藥物的治療窗口和效果相比第一代改善。而第三代ADC藥物主要的技術突破是定點偶聯技術的發展,提升了抗體偶聯比(DAR)均一性,進一步降低毒副作用並增強療效,治療窗口持續提升。同時,抗體優化和新型小分子也加強了藥物的特異性和治療效果,並對抗原水平表達較低的細胞具有結合活性。
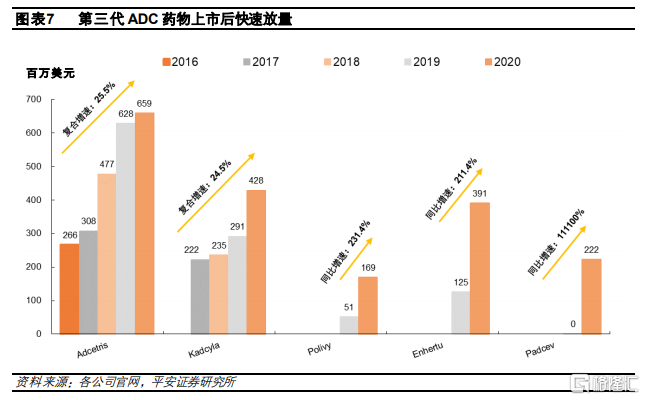
1.3 上市ADC藥物銷售持續放量
第三代ADC藥物上市後實現快速放量。目前已上市的12款ADC藥物中,3款第三代ADC藥物Polivy、Enhertu和Padcev在2020年均實現快速放量,分別實現收入1.69、3.91和2.22億美元,同比增長231%、211%和111100%,主要是由於其療效相比現有治療手段提升顯著,同時填補了部分空白適應症,爲患者帶來新的治療選擇。而上市較早的第二代ADC藥物Adcetris和Kadcyla增速呈現放緩的趨勢,此外,這兩款藥物未來還要面對生物類似藥和技術迭代的競爭,增速可能會進一步放緩。伴隨ADC技術的持續發展,我們認爲ADC行業有望出現更多的重磅藥物品種,革新部分疾病領域的現有治療方法。
02
ADC研發火熱,市場具有較大潛力
2.1 ADC市場具有較大發展空間
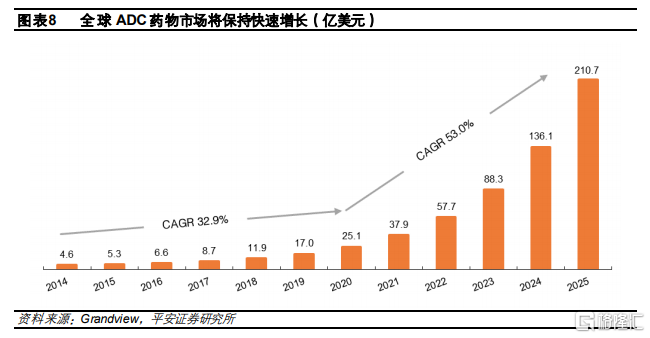
全球ADC藥物市場保持快速增長。根據Grandview數據,2014年全球ADC藥物市場規模爲4.6億美元,隨着上市藥物增加,到2020年全球ADC藥物市場已增長至25.1億美元,複合增速約爲32.9%。而隨着效果更好並且安全性更高的ADC藥物陸續上市,同時適應症拓展到更多疾病領域,ADC藥物的行業規模未來仍將保持快速增長,預計2020-2025年複合增速將超過50%。
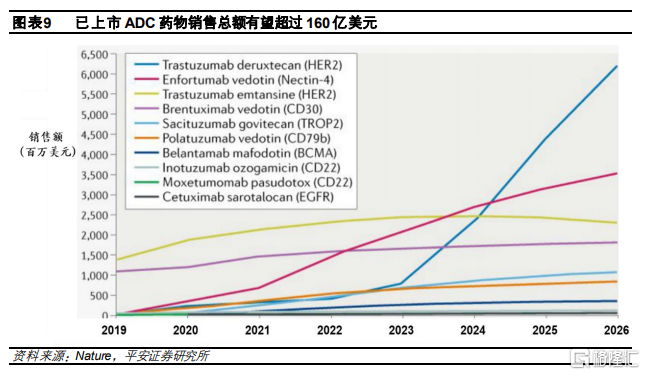
已上市ADC藥物仍有較大市場潛力。根據Nature文章測算,2020年以前上市的10款ADC藥物到2026年其銷售總額將超過164億美元。其中,由於療效突破顯著和適應症豐富,第一三共的Enhertu預計將以62億美元的銷售額位居第一位,佔據約40%的市場份額。而Roche的Kadcyla由於僅限於治療HER2+乳腺癌並且將面臨生物類似藥的衝擊,其2026年銷售額預計爲23億美元。伴隨ADC開發技術的進步,未來將涌現更多相比現有療法效果更顯著的重磅藥物,賽道具有較大發展潛力。
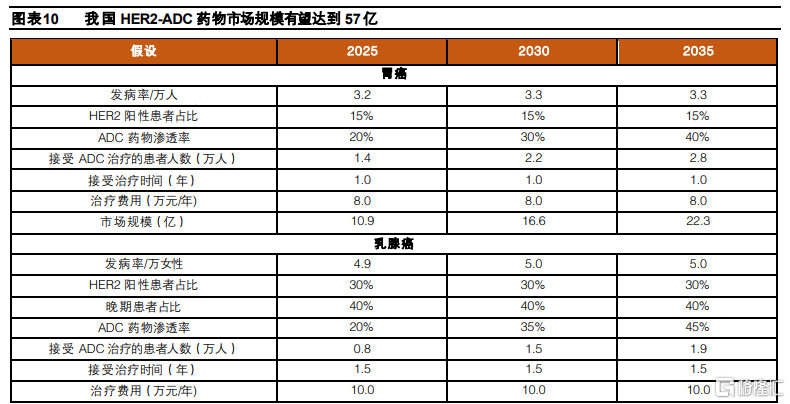
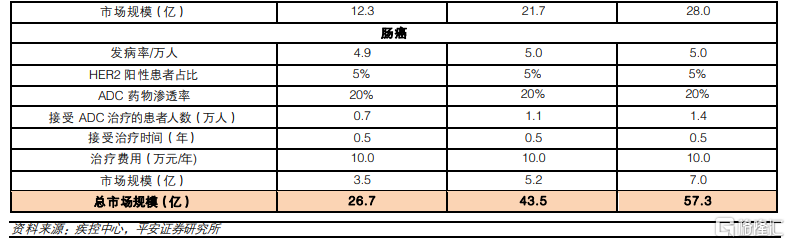
我國HER2-ADC藥物市場規模有望超過50億元。目前我國進度較快的ADC藥物主要是針對HER2靶點,適應症主要集中在乳腺癌、胃癌和腸癌,以這3個適應症進行測算,我們預計,我國HER2-ADC藥物的市場空間在2025年有望達到26.7億元,到2030和2035年有望達到43.5和57.3億元。考慮到ADC藥物目前已經在後線治療中展現顯著療效,填補部分後線適應症的治療空白,爲患者帶來更多治療選擇,同時有望取代部分現有療法,市場具有較大市場前景。
2.2 ADC藥物集中在實體瘤領域,並多爲成熟靶點
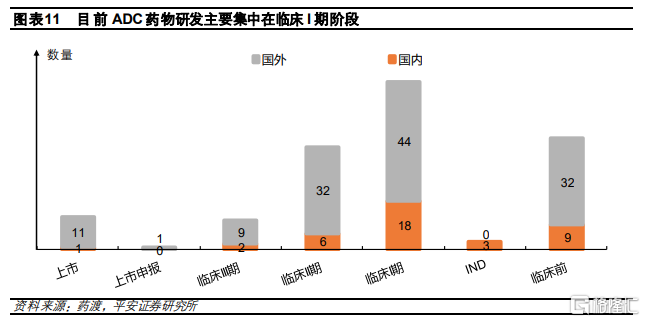
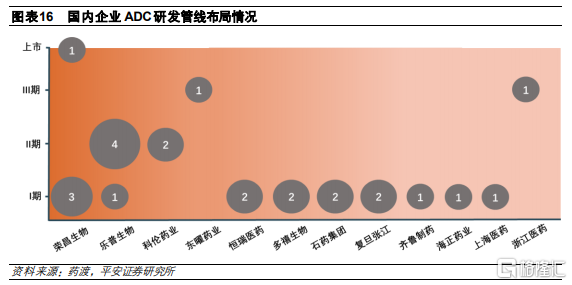
國產ADC藥物有望在3-5年迎來收穫期。由於ADC治療效果較好,市場具有較大發展潛力,因此全球範圍內研發熱度較高。根據藥渡不完全統計,目前全球共有156款ADC藥物處於臨牀研發階段,其中,11款處於臨牀III期階段,多數處於臨牀I期階段。由於我國ADC藥物研發起步相對較晚,目前共有38款ADC藥物,多數仍然處於臨牀I期和臨牀前階段,與國外相比進度較爲落後,有望在未來3-5年迎來上市收穫期。
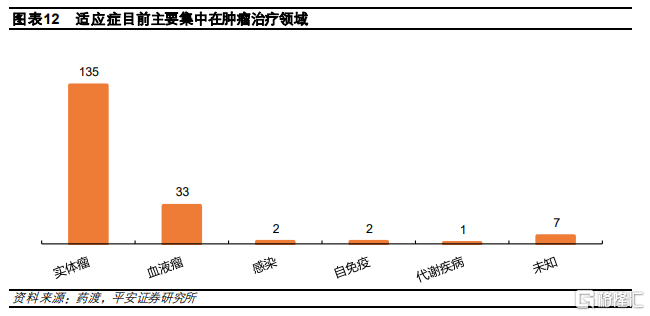
目前ADC適應症主要集中在實體瘤領域。從在研ADC藥物的適應症佈局來看,全球ADC藥物研發主要集中在腫瘤領域,其中實體瘤最爲熱門,共有135款ADC產品在研,佔全部管線約87%。伴隨抗體篩選技術和基因工程技術的進步,ADC藥物的特異性和穩定性增強,安全係數提升,適應症也逐漸從腫瘤治療往其他疾病方向發展,目前已拓展至感染、自免疫以及代謝疾病等。
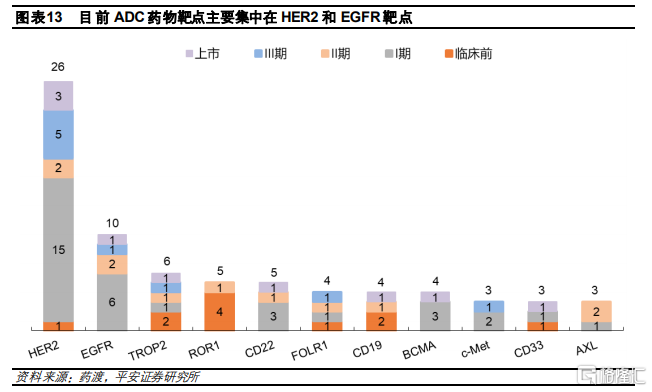
ADC靶點選擇主要集中在成熟的已驗證靶點。從靶點佈局來看,目前ADC藥物研發集中在成熟靶點,主要是已有上市ADC藥物或者已在其他療法中得到驗證的靶點。其中,上市藥物數量最多同時在研藥物數量最多的是HER2靶點,一共有26款。排名第二的熱門靶點是EGFR,目前已有1款藥物上市,同時還有6款藥物處於臨牀I期。這兩個靶點賽道相對較爲擁擠。
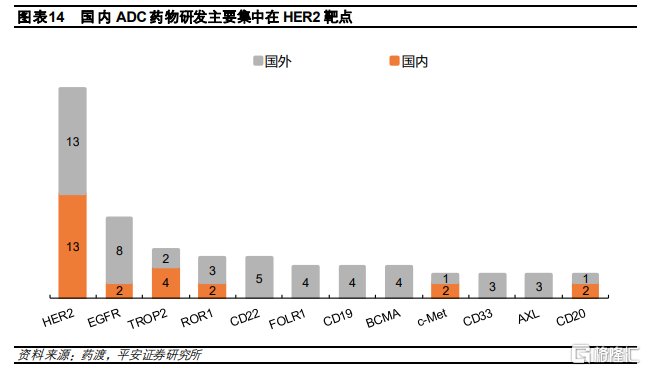
國內HER2-ADC賽道較爲擁擠。國內的ADC藥物研發主要集中在HER2和TROP2靶點,其中,HER2賽道最爲擁擠,目前共有13款產品,佔國內ADC管線約34%。但是國內企業也開始佈局尚未有產品上市的靶點,例如c-Met、ROR1、MUC1等,但是與國外相比,靶點選擇仍然較爲單一,研發同質性相對較高。
整體來看,目前ADC藥物部分靶點賽道已經較爲擁擠,產品上市就將面臨較爲殘酷的競爭格局。但伴隨技術進步,部分ADC研發企業也開始逐步探索創新靶點,該類靶點賽道尚未形成明顯競爭格局,仍然有較大的發展潛力,有望出現重磅品種。
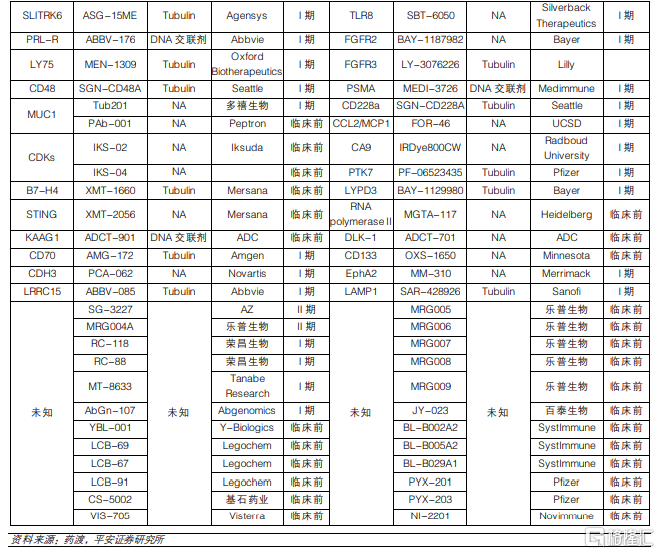
2.3 企業通過自研或合作等方式佈局ADC賽道
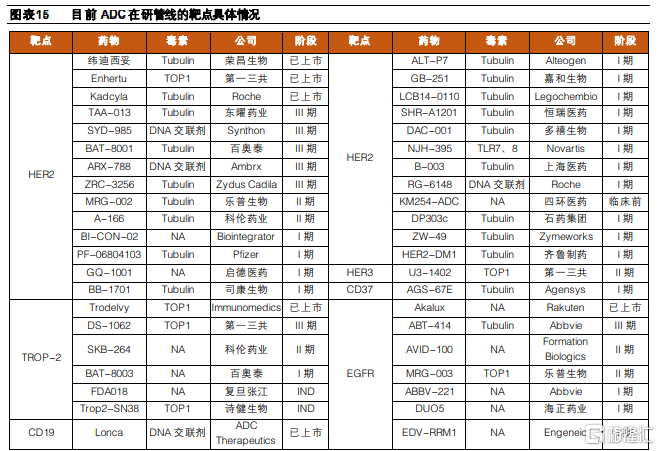
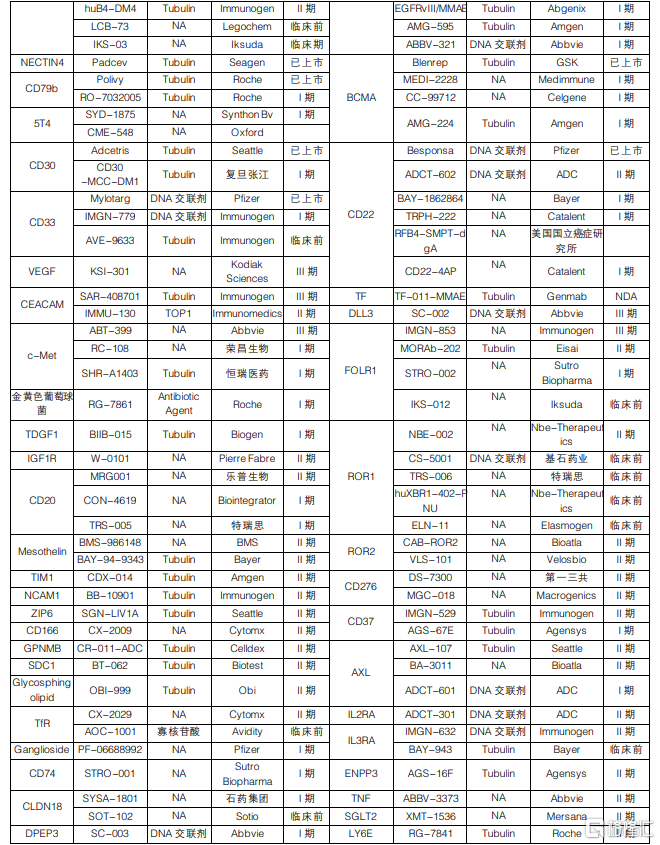
榮昌生物擁有首款國產上市ADC藥物。從目前企業的佈局情況來看,國外企業由於起步較早,因此ADC研發管線較爲豐富,Roche、Seagen、第一三共等企業均有產品上市,並且仍有較爲豐富的在研產品佈局。國內企業方面,擁有較多ADC藥物佈局且已進入臨牀後期的企業主要有榮昌生物、樂普生物和東耀藥業等,其中,榮昌生物的維迪西妥單抗已於2021年6月獲批上市,成爲國內首款上市的國產ADC藥物。國內其他企業的ADC管線仍然處於早期臨牀階段。
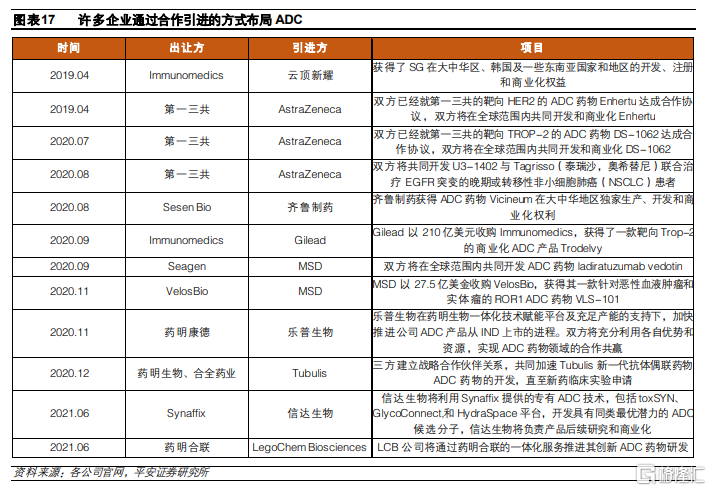
除了自主研發外,爲快速搶佔賽道,國內外各大企業也通過合作研發以及授權引入等方式對ADC藥物管線進行佈局。
03
ADC影響因素較多,具有較高研發壁壘
3.1 ADC由三要素組成,研發壁壘較高
ADC藥物在體內需要經歷複雜生物過程才能發揮作用。ADC自概念提出至今已超過100年,但是上市品種仍然較少且在研品種多數仍處於早期的主要原因是ADC藥物開發難度較大,技術壁壘較高。ADC藥物在進入體內後需要經過多個步驟才能生效,每個步驟都有需要克服的技術難點:
1)藥物到達細胞表面識別結合抗原,這一步對細胞表面抗原的密度和腫瘤特異性有較高要求;
2)ADC-抗原複合物被細胞內化,要求ADC藥物具有較高的內化效率;
3)ADC藥物被溶酶體降解並釋放毒素,這一步需要有效載荷能夠快速脫落並且從溶酶體逃逸;
4)毒素觸達細胞內藥物靶標從而殺死細胞,這一步需要毒素具有較強毒性能夠殺死細胞;
5)細胞死亡並釋放毒素殺傷鄰近細胞,這一步需要毒素能夠穿過細胞膜從而發揮旁觀者效應。
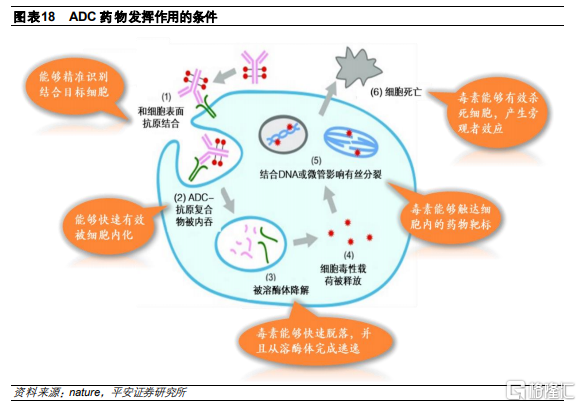
ADC藥物的構建核心主要包括三要素和組合技術。ADC由三個部分組成,每個部分都能影響ADC最後的療效和安全性。爲了使ADC藥物能夠高效通過細胞內的生物過程從而發揮作用,在構建ADC時需要綜合考慮抗體、毒素分子、連接子及偶聯方式:
抗體:是ADC的精確制導部件,將毒素分子帶到腫瘤細胞,其選擇取決於疾病的靶標,可以分爲特異性抗原和相關性抗原
毒素:是影響 ADC 活性的關鍵因素,也是主要用於殺傷腫瘤細胞的有效分子,需要具備高毒性、高親和力和低免疫原性
連接子:起到連接作用,需要在血液循環中足夠穩定,而在到達靶細胞表面或進入細胞後能夠將小分子毒素有效釋放
連接方式:控制偶聯小分子的位置和數量,保障均一的藥物/抗體比率(DAR),穩定ADC藥物在體內的分佈代謝
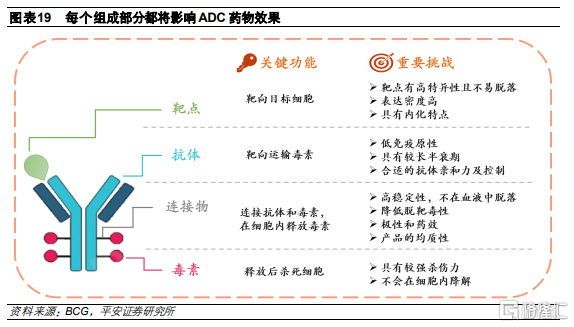
連接物-毒素化合物及偶聯方式是核心要素。在整個ADC構建中,容易產生差異性和專利的核心部分是連接子和毒素的組合部分,及其與抗體的偶聯方式。ADC藥物的抗體選擇是無限的,而目前連接物、連接方式及毒素的種類是有限的。作爲核心要素,連接物-毒素化合物已經被藥企申請了專利,各家擁有自主平臺的企業均有較爲獨特的設計,並且可以應用到多種ADC產品中。
3.2 靶點的選擇影響ADC藥物治療窗口
ADC對靶點的選擇具有較高要求。在確定了目標適應症後,首先需考慮的是哪些抗原在該類腫瘤細胞表面具有特異性且高水平的表達。靶點是ADC藥物主要識別腫瘤細胞和被內吞的主要媒介,其適用性是ADC藥物治療窗口和效果的關鍵決定因素之一,並且將影響藥物的成藥性和競爭格局。由於ADC藥物發揮作用的機制和現有療效均有差異,因此對於靶點特性的要求較爲特殊:
具有腫瘤特異性。爲了減少脫靶毒性,靶點應該在腫瘤細胞上具有排他性或優先性表達,而在正常組織上不表達或者低表達。例如,HER2受體在腫瘤上的表達量約爲正常細胞的100倍。
在腫瘤細胞表面大量表達。ADC藥物通過血流到達腫瘤細胞並識別表面抗原從而發揮作用,因此靶點需要在腫瘤細胞表面穩定且大量表達以便循環ADC結合使用,抗原密度應以高拷貝數(>105 /細胞)存在。
抗原應是不分泌型的。分泌型抗原可與體內循環系統中的ADC藥物或裸抗結合,從而導致與腫瘤細胞結合的ADC 藥物減少,影響藥物的療效和安全性。
可以被有效內化。ADC藥物在結合靶點後需要通過受體介導的內吞作用進入細胞,並且應進行適當的細胞內運輸和降解,從而釋放細胞毒性彈頭。細胞表面的靶抗原可能具有不同的基礎和抗體誘導內化率,這會影響ADC功效,不充分或低效的內化可能會增加脫靶毒性。
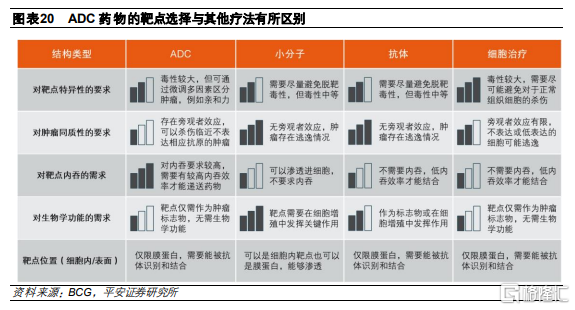
ADC藥物研發正在持續拓展靶點選擇。根據全球在研管線趨勢,目前處於研發階段的ADC藥物中,研發熱度最高的主要是腫瘤特異性較高並且已有上市產品的成熟靶點,例如實體瘤中的HER2、TROP2、Nectin4、EGFR,以及血液瘤中的CD22、BCMA、CD19和CD20等,這類得到驗證的靶點賽道已較爲擁擠。伴隨基礎研究的推進,目前ADC靶點的選擇逐漸開始向創新靶點延伸,並基於藥物作用機制的特殊性,開始探索ADC特有靶點。
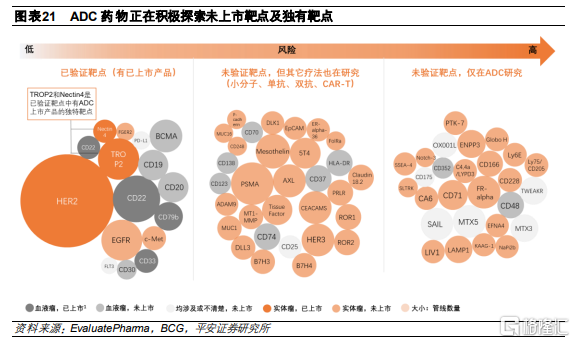
腫瘤微環境相關靶點的耐藥性突變更少。從靶點類型來看,除了在腫瘤細胞上特異性表達的靶點,腫瘤微環境相關的靶點也成爲了研發熱點,包括新血管系統、內皮下細胞外基質和腫瘤基質中的抗原。靶向基質的ADC通過降低基質產生的生長因子的濃度導致腫瘤細胞死亡。由於所有腫瘤細胞的存活都依賴於血管生成和基質因子,因此靶向此類組織的ADC可能具有更廣泛的功效。此外,這些細胞與腫瘤細胞不同,其基因組相對較爲穩定,產生耐藥性突變的可能性相對較小。
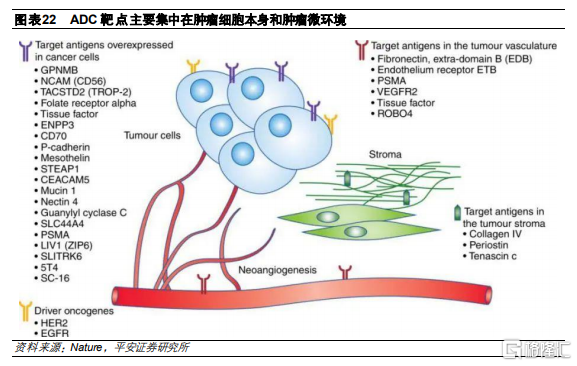
3.3 抗體的選擇影響ADC藥物內吞效率
在選定了靶點後,爲ADC選擇合適的抗體也很重要,會對療效、藥代動力學/藥效學特徵和治療指數產生重大影響。用於ADC的理想抗體應該具有很強的目標結合親和力。此外,它還應具有高穩定性、低免疫原性、高效內化和長血漿半衰期。
免疫原性主要和抗體來源相關。在ADC藥物剛開始研發時,主要使用的仍然是鼠源性抗體,較強的免疫原性導致副作用較大,研發失敗率較高。伴隨抗蛋白工程和基因工程的技術進步,抗體也逐漸向人源化方向發展,免疫原性持續降低,目前已經能做到全人源化,提升了ADC藥物的研發效率。在已上市ADC藥物中,僅Adcetris使用嵌合抗體,其他上市藥物以及目前正在開發的大多數ADC使用人源化或人單克隆抗體。
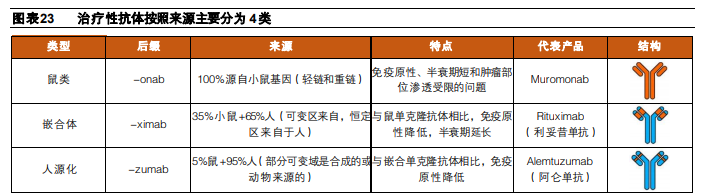
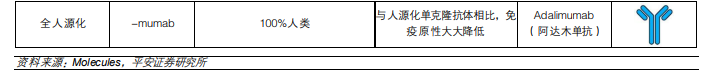
抗體的半衰期和效應子功能與抗體亞型相關。目前IgG是主要用於開發治療藥物的抗體類型,而在IgG的4種亞型中,IgG1是目前最常用的類型,這主要是IgG1相比其他亞型具有一定優勢:
IgG1和IgG3與Fc受體的親和力高於IgG2和IgG4,具有更強的激活抗體依賴的細胞毒性(ADCC)及補體依賴的細胞毒性(CDC)效應,而IgG2和IgG4有阻礙或抑制的效應功能;
而IgG3由於與Fcγn的受體結合率較低,導致其清除速度較快,半衰期約爲7天,因此較少被應用,而其他亞型在血清中的穩定性相似,半衰期約爲21天;
IgG2雖然也可以有效觸發補體效應,但會形成二聚體,可能導致聚集並導致ADC無效;
IgG4抗體可以形成新的雙特異性抗體,穩定性較低。當不需要募集宿主效應器功能時,IgG4是ADC開發的首選。目前上市的ADC中,Mylotarg和Besponsa使用的是IgG4抗體。
抗體內化效率主要和抗體對抗原的親和力相關。ADC使用抗體的親和力越高,內化效率越快,但具有極高抗原親和力的抗體會導致實體瘤穿透效率降低,會影響ADC藥物到達腫瘤內部的效率。因此,抗原必須以合理的親和力(Kd≤10 nM)被抗體識別和結合,以確保在靶細胞中快速吸收。同時,還需要考慮選擇的抗體分子量大小,當抗體分子量太大時,難以透過毛細管內皮層和細胞外間隙,抗體的分子量太小可能會影響其在體內的半衰期。
ADC抗體的優化方向主要是提高內吞和滲透效率。當前,缺乏療效和脫靶毒性是ADC藥物面臨的主要挑戰,其中一個重要原因便是到達腫瘤的ADC藥物較少和內化速率有限。目前研究人員正在開發解決提高遞送效率和內化速度的方法,如提高滲透率和使用雙特異性抗體的ADC藥物:
使用雙抗增強親和力和特異性。雙抗可以同時與同一靶細胞上的兩種抗原相互作用,這種特性可能會增加治療窗口,同時減少對非靶細胞的非特異性作用。此外,使用靶向兩個非重疊表位抗原的雙抗可以增強抗體對抗原的親和力,從而提高ADC藥物的內吞效率。
去掉Fc端提高滲透性。由於ADC藥物的尺寸較大,基質屏障和腫瘤組織滲透是ADC治療實體瘤需要克服的障礙。由於抗體在整個結構中結構佔比較大,因此目前方法主要是針對減小抗體分子量。例如使用scFv(可變區)或sdAb(納米抗體)作爲砌塊構建抗體,由於這兩個模塊分子量較小,構建出來的抗體相比IgG較小,能夠更快滲透進腫瘤。
旁觀者效應解決結合位點屏障。另一個可能導致腫瘤滲透性差的因素是結合位點屏障效應。這是一種現象,對血管附近的靶抗原具有高靶標親和力的抗體可能由於抗原的快速和緊密結合而在遠離血管的分佈較少,導致ADC藥物清除腫瘤效率下降。能夠改善滲透性和分佈的小尺寸 ADC 可使用“旁觀者效應”,對鄰近腫瘤細胞進行殺傷,解決位點屏障。
3.4 連接子的選擇影響ADC穩定性和效率
連接子會影響治療窗口。連接子是關係到藥物穩定性和治療窗口的關鍵之一。首先,連接子需要具備一定的穩定性,從而在未達到腫瘤細胞之前,能確保ADC在血液循環過程中的完整性,避免提前釋放毒素導致脫靶毒性,影響ADC藥物的治療窗口。而在進入靶細胞後,連接子要確保毒素的有效釋放,發揮殺傷作用。連接子從性能上可分爲不可裂解連接子和可裂解連接子:裂解型的連接子可利用腫瘤微環境特異性釋放小分子毒素;非裂解型是通過細胞內溶酶體斷開抗體和連接子的連接。
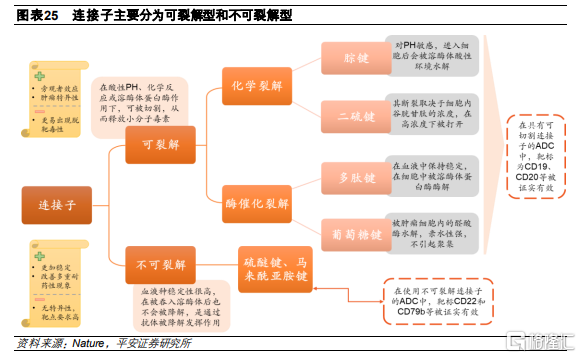
可裂解連接子根據裂解機理不同分爲:化學裂解連接子和酶裂解連接子,其中化學裂解連接子包括腙鍵和二硫鍵,酶裂解連接子主要包括葡萄糖鍵和多肽鍵。
1) 腙鍵:對pH值敏感。在血流中性pH下結構穩定,而在酸性細胞區室,例如溶酶體(pH 4.8)或晚期內體(pH 5.5-6.2)中會被水解釋放有效載荷。然而,該接頭在循環過程中並不穩定,在血液中會緩慢水解,存在毒素脫落,目前其應用主要侷限於血液瘤。
2) 二硫鍵:對谷胱甘肽敏感。血液中谷胱甘肽(GSH)的濃度爲5 µmol/L,遠低於細胞中谷胱甘肽的濃度(1–10 mmol/L),而腫瘤細胞會引起氧化應激,從而產生高 GSH 水平,促進有效載荷的釋放。因此,二硫鍵連接子在血液中非常穩定,並具有一定腫瘤特異性。
3) 葡萄糖鍵:對糖苷酶敏感,例如β-葡萄糖醛酸酶。含有β-葡萄糖醛酸的ADC可以達到DAR=8,而不會引起聚集,也不會降低 ADC 的疏水性。事實上,這種類型的接頭大大降低了 ADC 的血漿清除率,從而提高了它們在體內的功效
4) 多肽鍵:會被組織蛋白酶B酶解,這是一種溶酶體蛋白酶,在腫瘤細胞中過度表達,而在血液中存在蛋白酶抑制劑。因此,這種連接子在循環中高度穩定,而進入腫瘤細胞後會被溶酶體蛋白酶B酶解,以活性結構釋放細胞毒素,較好的保持了其的理化特性。
不可裂解連接子由穩定的鍵組成,在血循環和腫瘤細胞內均可保持穩定。
1) 比如硫醚連接子、酰胺類連接子。不可裂解連接子依賴於蛋白酶對ADC的抗體成分的酶解,最終釋放出與來自降解抗體的氨基酸殘基相連的有效載荷分子。因此,當與不可切割的接頭結合時,需要仔細選擇和設計有效載荷結構,以便有效載荷能夠以這種修飾形式發揮抗腫瘤效力。Roche的Kadcyla是通過穩定的硫醚連接子將DM1連接到抗體上。
旁觀者效應是兩種連接子的主要區別之一。不可裂解連接子必須在ADC的抗體被降解後釋放毒素,這種形式的ADC不會產生旁觀者殺傷,因爲通常連接子-毒素複合物的正電荷阻止其穿透細胞膜從而無法進入周圍細胞。而可切割連接子在細胞內或細胞外被降解後,釋放產生的遊離藥物將直接殺死靶細胞,並可以擴散出靶細胞以引起鄰近不表達靶抗原的細胞死亡,進一步增強腫瘤殺傷能力。
目前ADC藥物的藥物抗體比(DAR)限制較爲嚴格,有效載荷超過4就較易在血漿中聚集並被清除,而DAR的增加會直接影響ADC對於腫瘤的殺傷力,爲進一步提高藥物治療窗口,降低最低有效劑量,目前連接子的主要研發方向包括提高連接子的親水性和增加連接子上有效載荷的承載數量:
提高連接子的親水性。目前已證明 ADC 疏水性的增加與 ADC 清除率的增加有關,而 ADC 的清除率可以通過接頭-藥物設計進行修改,使用基於肽鍵的親水性接頭的Enhertu和聚乙二醇化 ADC 證實了這一點。因此,有望通過增加連接子親水性降低由於DAR增加導致的清除。
增加連接子上有效載荷的承載數量。迄今爲止開發的大多數ADC的連接子僅加載單個有效載荷。然而,最近的研究表明抗體可以與兩個以上的有效載荷相關聯。Anami及其同事最近報告了他們在分支連接子上的研究進展,該連接子可以加載多個有效載荷分子,提高藥物效力。
3.5 毒素的選擇影響ADC藥物效力
毒素是發揮腫瘤殺傷作用的組成部分。在ADC藥物進入細胞後,毒素是最終造成靶細胞死亡的主力軍,因此,毒素的毒性和理化特性會直接影響藥物對於腫瘤的殺傷能力,從而影響療效。用於偶聯的細胞毒素必須具有較爲清晰的作用機制、較小的分子量、較高的細胞毒性,並且採用化學方法偶聯到抗體上後仍能保留抗腫瘤活性。
具有較高細胞毒性。考慮到抗體較差的滲透能力和內吞效率,以及細胞表面較低的抗原表達量,最終能被遞送到靶細胞中的有效載荷數量有限。假設ADC作用機制中的每個步驟的效率爲50%,那麼只有1.56%的毒素能夠進入細胞並發揮作用,而人體中的實際數據更低。因此,爲了保障藥物作用,ADC選擇的毒素需要具有足夠高的毒性效力以有效殺傷腫瘤。
具有較小的分子量。ADC整體分子量增加可能會導致ADC藥物的聚集,使其被較快清除,因此,毒素的分子量應控制在合理範圍。此外,較小的分子量使得毒素可以透過細胞膜擴散到鄰近細胞,發揮旁觀者效應,進一步增加腫瘤清除效果。
作用機制較爲清楚。由於ADC藥物是通過被靶細胞內化發揮效果,因此毒素主要是在細胞內被釋放,需要靶向細胞內靶點,並通過凋亡機制誘導癌細胞死亡,因此作用機制需要明確。
採用化學方法偶聯到抗體上後仍能保留抗腫瘤活性。某些細胞毒素如長春花鹼和甲氨蝶呤偶聯到抗體上後幾乎失去抗癌能力,這類毒素就無法作爲有效載荷。
根據作用機制不同,目前用於ADC的細胞毒素主要分爲DNA損傷劑和微管蛋白抑制劑。
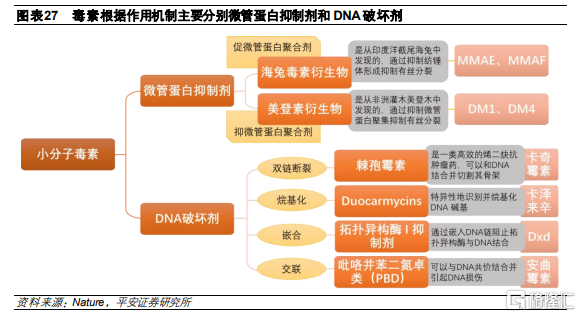
微管蛋白抑制劑
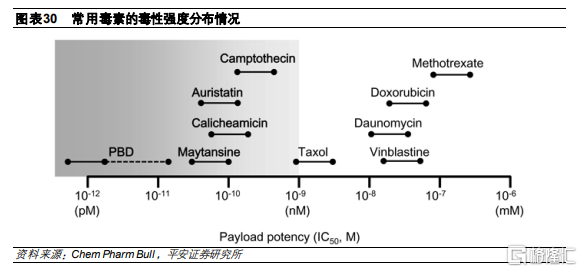
微管是細胞骨架的主要組成部分, 在細胞分裂過程中的起到重要作用。由於腫瘤細胞會保持快速增殖,因此,幹擾腫瘤細胞有絲分裂的微管蛋白抑制劑成爲腫瘤藥物研發方向之一。該類抑制劑主要是抑制微管蛋白的聚合或者促進微管蛋白的聚合。其中,促進微管蛋白聚合劑作用於α-β微管蛋白二聚體的β-亞基,使微管生長不受調控,如MMAE、MMAF。而抑制微管蛋白聚合劑是通過抑制成熟微管的形成來阻斷微管蛋白二聚體的聚合,如DM1、DM4。
DNA損傷劑
與微管抑制劑的納摩爾範圍相比,DNA損傷劑的IC50值僅爲皮摩爾,因此使用DNA損傷劑作爲有效載荷構建的ADC更有效,可以靶向在腫瘤上低水平表達的抗原,並且能夠殺傷處於任何細胞週期的靶細胞。DNA損傷劑分爲四種作用機制:(a) DNA雙鏈斷裂,例如卡奇黴素;(b) DNA烷基化,例如卡澤萊辛;(c) DNA嵌入,例如Dxd;(d) DNA交聯,例如安麴黴素。
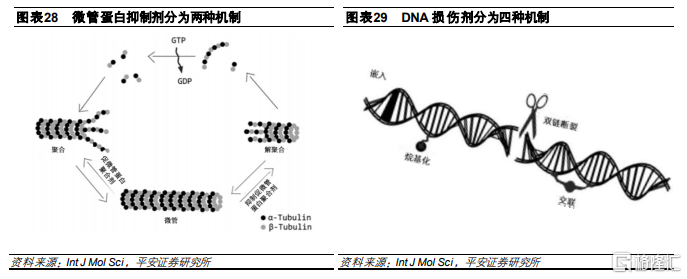
從毒素的IC50分佈情況來看,ADC毒素至少要到nM級別。目前較爲常用的這幾種細胞毒素中,美登素相比海兔毒素毒性較大,而毒性最大的目前是DNA破壞劑中的PBD,是相對較爲有效的有效載荷之一。PBD殺死癌細胞的作用方式是與癌細胞DNA的特定靶標結合並交聯。因此,這可以防止腫瘤細胞增殖而不使其 DNA 螺旋變形,從而有可能避免出現耐藥現象。
3.6 偶聯方式的選擇影響ADC藥物均一性
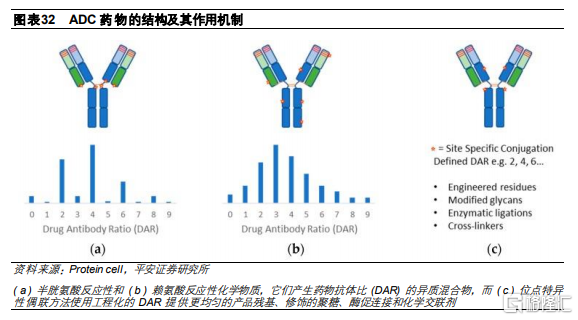
偶聯方式是最後的關鍵環節。在決定了抗體、連接子和細胞毒素之後,三者的偶聯方式會影響藥物抗體偶聯比(Drug Antibody Ratio,DAR)及ADC藥物的均一性,從而影響ADC的生物學活性、耐受性及藥物穩定性。如果偶聯的細胞毒素過少,則會降低其生物活性和療效;過多則增加ADC在血液中的清除率及安全性風險,同時影響抗原和抗體的有效結合。通常而言,理想的DAR爲2-4。目前已進入臨牀的ADC藥物所使用的偶聯方式主要分爲隨機偶聯和定點偶聯。
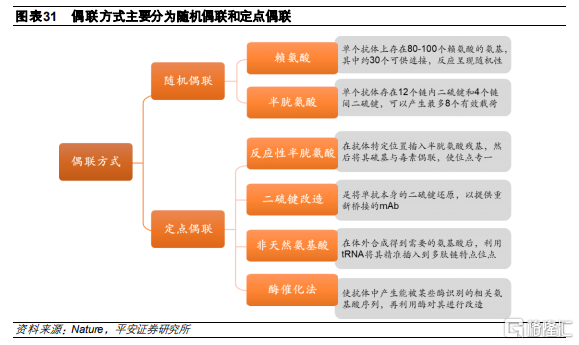
隨機偶聯和定點偶聯的主要區別是抗體DAR分佈情況。DAR可能在0-8之間變化,因此,使用隨機偶聯會產生具有不同DAR的ADC的異質混合物,導致最終成品中ADC藥物的有效性不一,影響藥物整體療效和劑量。而定點偶聯的DAR較爲明確,最終成品的一致性較高,提高治療窗口。
隨機偶聯:目前已上市的藥物基本都是使用隨機偶聯,會產生具有不同DAR的ADC的異質混合物,其藥代動力學、活性和安全性各不相同,導致療效下降。抗體上的半胱氨酸( 8個) 和賴氨酸殘基( 80個) 較易發生化學反應而被修飾,因此常作爲與效應分子結合的位點。
a) 賴氨酸酰胺偶聯
在早期ADC的開發研究中,通常選擇抗體上的賴氨酸作爲結合位點,其合成效率較高。但由於每個抗體上的賴氨酸殘基可達80個,導致了很大的異質性,平均DAR爲3.5-4,分佈在0-7之間,影響ADC藥物的體內分佈和細胞毒性,Kadcyla就是使用這種方式。
b) 半胱氨酸偶聯
每個抗體上只有8個遊離的半胱氨酸可通過二硫鍵與連接子連接,由於結合位點的數量有限和硫醇基團的獨特反應性,用半胱氨酸作爲連接位點有助於降低ADC的異質性。產生的DAR爲2、4、6、8,相對優於賴氨酸,代表藥物有Adcetris。
定點偶聯:隨着基因技術的發展,通過基因工程在抗體分子中引入具有活性基團的氨基酸,從而通過氨基或巰基的化學定點偶聯毒素,實現對於DAR及產品均一性的有效控制。
a) 反應性半胱氨酸偶聯(Thiomab技術)
最早由Genentech開發,在抗體兩個重鏈上引入新的半胱氨酸殘基,用於選擇性抗體附着。這種經過改造的半胱氨酸技術能夠穩定生成DAR爲2的高度同質(佔比高達92.1%)ADC。而在此基礎上,新的方法不斷提升DAR,包括通過將半胱氨酸殘基進行硫醇芳基化和使用二溴重新橋接二硫鍵,這兩種方法將得到DAR分別爲4.4和4的ADC。
b) 糖基化連接
由於IgG是一種糖蛋白,它在Fc片段每個重鏈的CH2結構域N297位置包含一個N-聚糖,這種糖基化可以作爲連接有效載荷的附着點。多糖與Fab區域間遠距離定位降低了在偶聯後損害抗體的抗原結合能力的風險,此外,與抗體的肽鏈相比,它們的化學組成不同,允許位點特異性修飾,使它們成爲合適的偶聯位點。
c) 非天然氨基酸
通過在抗體中引入β-乙酰苯丙氨酸作爲非天然氨基酸殘基,其含有天然氨基酸中不含有的酮官能團。酮官能團與烷氧基胺間可形成肟鍵,該鍵在生理條件下非常穩定。
d) 酶催化
有效載荷的附着可以通過在抗體序列中插入特定的氨基酸標籤以非常有選擇性的方式實現。這些標籤被特定的酶所識別,例如甲酰甘氨酸生成酶(FGE)、微生物谷氨醯胺轉胺酶(MTG)、轉肽酶或酪氨酸酶,從而能夠執行位點特異性偶聯。
04
全球主要技術平臺及管線佈局情況
4.1 國內ADC研發正在向創新邁進
隨着Kadcyla等第二代ADC藥物在全球上市,展現出較好的臨牀療效和市場銷售,國內部分企業也開始啓動ADC藥物開發,但主要以me-too爲主,佈局國外已有上市藥物的成熟靶點,例如HER2。參考PD-1競爭格局,未來部分國產ADC藥物有可能也要面臨較爲殘酷的競爭,速度較爲靠前的企業具有先發優勢,有望快速搶佔市場份額。伴隨加入賽道的企業數量增加,以及國內開發技術的進步,部分企業開始探索具有差異化的ADC藥物,主要體現在靶點和ADC組合要素及技術的選擇。未來我們認爲我國ADC藥物研發有望進入創新階段,引領全球創新。
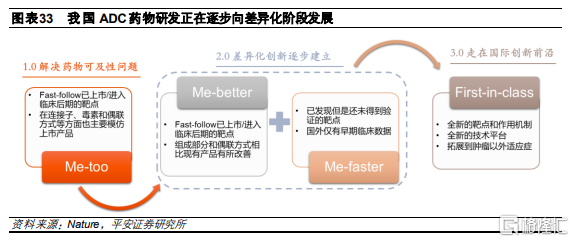
HER2-ADC藥物研發驗證了發展趨勢:
模仿:我國藥企最開始主要是對Kadcyla進行me-too模仿,例如BAT8001(百奧泰)、TAA013(東曜藥業)等,從靶點到技術路徑幾乎一致,均是使用曲妥珠單抗、不可裂解的MCC連接子、美登素類似物的毒素和賴氨酸隨機偶聯方式。
超越:隨後,我國部分企業開始在Kadcyla基礎上對部分組成要素進行改善,例如維迪西妥單抗(RC48,榮昌生物)。在抗體端,維迪西妥採用了篩選優化後的新型HER2單抗,相比曲妥珠單抗具有更高親和力。在連接子端,採用了酶裂解連接子,基於“旁殺效應”提高對腫瘤組織的整體殺滅效果,並具有更好的穩定性。在偶聯方式上採用了胱氨酸隨機偶聯,相比賴氨酸具有更好均一性,毒素也從美登素類似物改爲MMAE。
創新:伴隨我國技術進步,現在國內部分企業在新型毒素和定點偶聯方式上發力,進一步改善藥物的均一性和安全性。例如MRG002(樂普生物)和A166(科倫藥業)等,使用了定點偶聯技術,提高整體均一性和有效性,有望能夠對Kadcyla耐藥或無效的人羣產生療效。
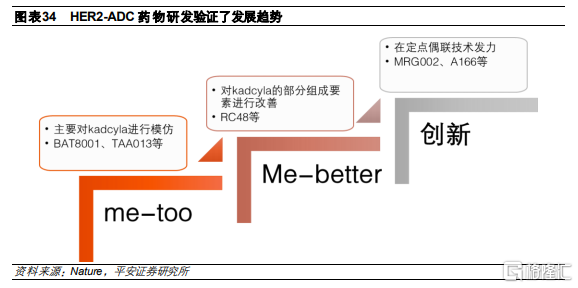
臨牀數據驗證ADC分子創新的重要性。從目前HER2-ADC效果來看,第三代創新型ADC藥物,例如第一三共研發的Enhertu、浙江醫藥的ARX788和科倫藥業的A166,憑藉其較強的分子創新設計,目前已在臨牀中取得了較爲顯著的療效結果,驗證了第三代ADC藥物的相對優勢。同樣,相比Kadcyla分子進行改良的ADC藥物,例如維迪西妥,也在後線治療中取得了較爲不錯的臨牀結果。
ADC平臺是企業管線擴張的關鍵。ADC作爲一種組合型藥物,任何一個組成部分都可以進行替換更改,不僅是抗體+毒素的模式,還可以是抗體+抗生素、抗體+趨化因子、抗體+TLR激動劑等模式。因此,ADC組合技術平臺具有較大的外延價值,可以組合迭代出豐富的產品,有望賦能企業產品管線開發,擁有自主研發平臺的企業有較大的發展潛力。參考國際領先ADC企業的發展歷程,例如第一三共和Seattle,均是先有優勢平臺立身,通過拓展多種盈利模式壯大。
4.2 第一三共
第一三共集團是一傢俱有百餘年曆史的跨國製藥企業,總部位於日本東京,全球約有1.5萬名員工。是在全球範圍內專業從事各類醫藥產品的研究、開發、生產和經營的多元化製藥集團。公司的ADC技術平臺稱爲DXd ADC,在ADC的有效載荷和連接子上作出了多項技術創新,包括:
使用的創新DNA拓撲異構酶I抑制劑(DXd)具有獨特作用機制,與常用的化療藥物伊立替康(SN-38)相比,活性提高10倍 ,具有更強的殺傷作用,並且相比Kadcyla耐藥性更少。此外,DXd具有很強滲透細胞膜的能力,能夠產生旁觀者效應;
在連接子方面,公司使用的連接子有着非常高的穩定性,能夠特異性被腫瘤中高度表達的溶酶體蛋白酶(cathepsins)切割,讓非腫瘤組織不會受到毒性藥物的影響;
公司使用的偶聯技術可以在一個抗體上穩定偶聯多個有效載荷,開發了能夠在將DAR控制爲4的富集技術,幫助獲得療效和安全性之間的平衡。
利用專有的技術平臺,公司目前已經開發了7款ADC藥物,其中Enhertu(DS8201)已經完成上市,其他幾款仍然處於研發階段。

Enhertu (DS8201)
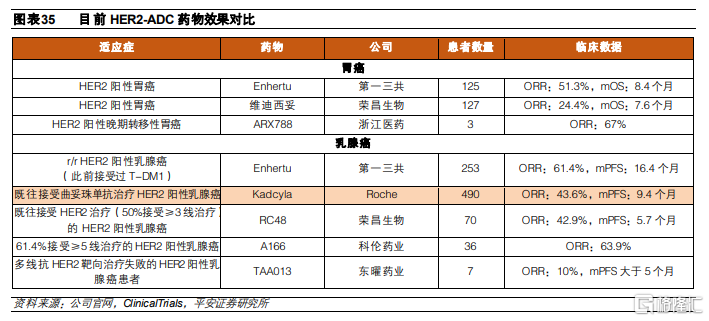
Enhertu(DS-8201)是公司開發的HER2-ADC藥物,由人源化曲妥珠IgG1單抗、拓撲異構酶I抑制劑和酶促裂解四肽連接子(GGFG)組成,採用的偶聯方式是半胱氨酸殘基的定點偶聯。
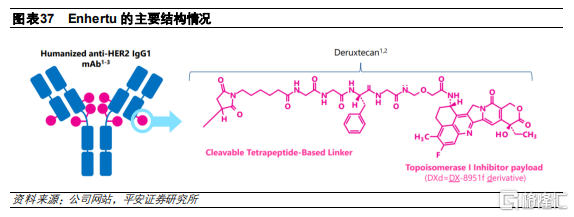
Enhertu和相比目前已批準的ADC具有更高的DAR,達到8,這是常規鏈間半胱氨酸偶聯的最大載藥量。較大的DAR使得Enhertu能夠對低 HER2 表達水平的腫瘤產生抗腫瘤作用,適應症相比Kadcyla得到進一步拓展。然而,DAR爲8的ADC藥物具有較高構建難度,主要是由於DAR大於4會使得ADC藥物出現聚合,第一三共通過降低連接子疏水性從而使得藥物在DAR爲8的情況下保持穩定,從而降低血漿清除率。
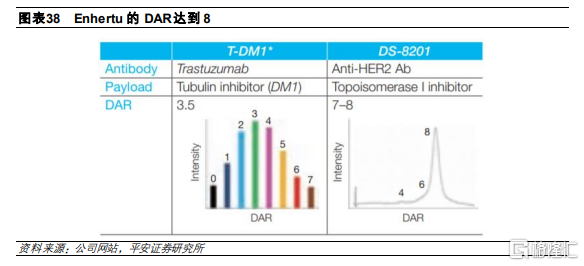
目前Enhertu已經在美國和歐洲獲批上市,適應症分別爲3線治療HER2陽性胃癌和3線治療HER2陽性乳腺癌。此外,還在開展多項臨牀試驗,拓展適應症,包括HER2低表達的腫瘤和HER2陽性非小細胞肺癌等。Enhertu已經在臨牀上展現顯著的療效,成爲HER2陽性腫瘤的重磅新藥。
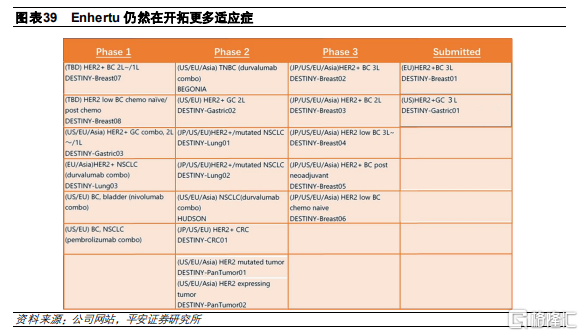
二線HER2陽性胃癌(DESTINY- Gastric01)
這是一項II期、開放的臨牀試驗,共招募187名此前接受過治療的HER2高表達胃癌患者。患者被分爲兩組,分別接受Enhertu和化療治療。Enhertu入組125名患者,治療方案爲6.4mg/kg Q3W,化療組入組62名患者,接受伊利替康/紫杉醇治療。從臨牀結果來看,化療組患者的ORR和mOS分別爲14.3%和8.4個月,而Enhertu組患者的ORR和mOS分別爲51.3%和12.5個月,療效提升顯著。
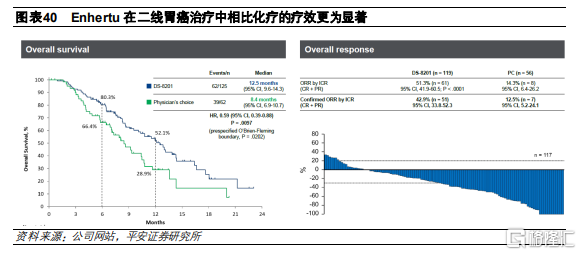
HER2陽性乳腺癌(DESTINY-Breast01)
這是一項II期、開放的臨牀試驗,共招募253名此前接受過Kadcyla治療的復發/難治性HER2陽性乳腺癌患者。患者被分爲3組,分別接受5.4mg/kg Q3W (184名)、6.4mg/kg Q3W(48名)和7.4mg/kg Q3W(21名)的治療方案。治療結果顯示,184名接受了5.4mg/kg Q3W治療方案的患者中,ORR達到61.4%,DCR達到97.3%,mPFS爲16.4個月,響應時間的中位數爲20.8個月,目前一線治療(曲妥珠+帕妥珠+化療)的整體響應時間爲20.2個月。該臨牀結果展現出Enhertu在對Kadcyla無響應羣體中的治療潛力。
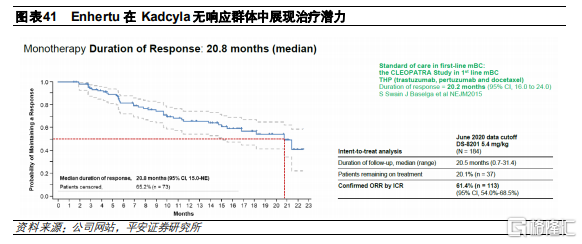
HER2陽性轉移性腸癌(CRC01)
這是一項II期、開放的臨牀試驗,共招募86名既往接受過兩線及以上標準治療的HER2陽性、不可切除和/或轉移性結直腸癌患者,其中包括53名HER高表達患者,15名HER2中表達患者和18名HER2低表達患者,接受6.4mg/kg Q3W的治療方案。在53名HER高表達的患者羣體中,ORR達到45.3%,DCR爲83.0%,mPFS爲6.9個月,OS爲15.5個月,療效顯著。而在其他兩個患者羣組中,ORR爲0。
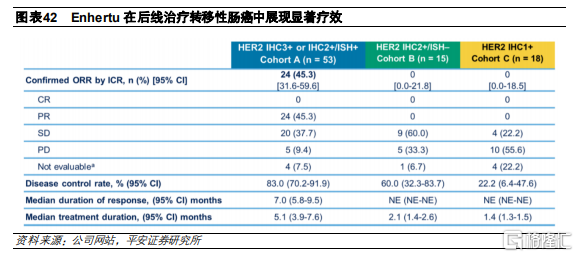
HER2突變肺癌(DESTINY- Lung01)
這是一項II期、開放的臨牀試驗,共招募42名HER2突變型轉移性非小細胞肺癌患者,接受6.4mg/kg Q3W的治療方案。根據臨牀數據顯示,患者ORR達到61.9%,DCR爲90.5%,mPFS達到14.0個月。由於療效較爲顯著,Enhertu基於該結果被美國FDA授予用於治療HER2突變轉移性非小細胞肺癌的突破性療法認定。
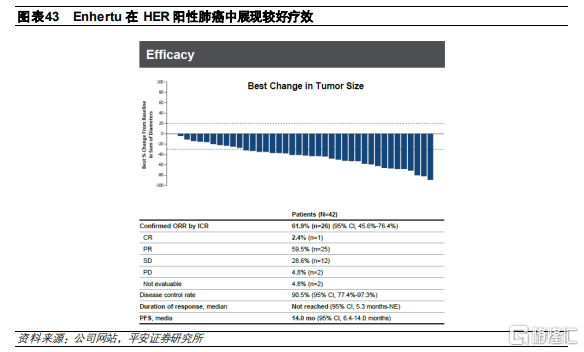
三陰乳腺癌(BEGONIA)
這是一項Ib/II期、開放的臨牀試驗,預計招募200名轉移性三陰乳腺癌患者,接受Enhertu(5.4mg/kg Q3W)和Durvalumab(1120 mg Q3W)的聯合治療方案。根據臨牀數據顯示,患者的ORR達到66.7%,反應具有持續性。
和Opdivo聯合治療HER2高表達乳腺癌
這是一項Ib期臨牀試驗,共入組48名HER2乳腺癌患者,其中包括32名接受過Kadcyla治療的HER高表達患者和16名接受過標準治療的低表達患者,接受Enhertu(5.4mg/kg Q3W)+Nivolumab(360mg Q3W)的聯合治療。臨牀數據顯示,高表達患者和低表達患者的ORR分別爲59%和38%,DCR分別爲91%和75%。
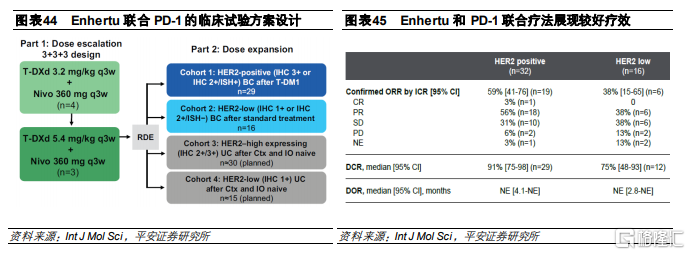
安全性研究
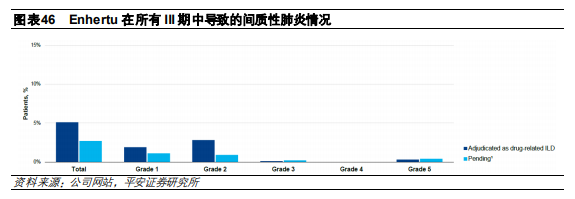
雖然Enhertu療效較好,但在臨牀中出現較嚴重副作用,主要是會造成間質性肺炎,並且在CRC01臨牀實驗中導致了3例和治療相關的死亡案例,這是其他HER2-ADC中所沒有觀測到的。公司整理了自臨牀試驗開展至2020年11月,所有III期單藥臨牀試驗發生的間質性肺炎情況。數據顯示,與治療相關間質性肺炎的發生率約爲總入組患者人數的5%,主要集中在一級和二級,但也有部分患者達到五級程度,安全性相對可控。
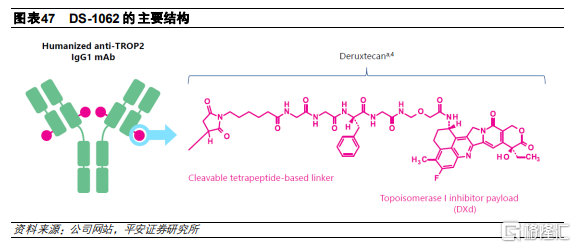
DS-1062
DS-1062是公司自主開發的TROP2 ADC藥物,由人源化抗TROP2的IgG1單抗、拓撲異構酶I抑制劑和酶促裂解四肽連接子(GGFG)組成,採用的偶聯方式是半胱氨酸殘基的定點偶聯,DAR爲4。
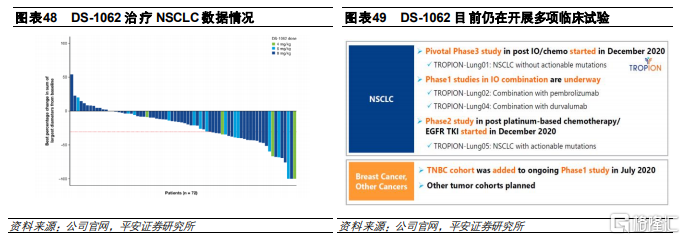
DS-1062目前正在進行臨牀III期關鍵性註冊臨牀,適應症爲經I/O和化療治療後難治或複發性的轉移性晚期非小細胞肺癌。公司此前在WCLC19上公佈了DS-1062的臨牀數據。在這項臨牀試驗中,共入組40個晚期NSCLC患者都經過包括EGFR、ALK抑制劑和免疫檢查點抑制劑在內的反覆治療,所有患者平均經過 3.5種方案的治療。臨牀數據顯示,已有12名患者出現部分緩解(PR爲30%,給患者帶來了更多治療選擇。此外,DS-1062還在開展三陰乳腺癌適應症。
U3-1402
U3-1402是公司自主開發的HER3 ADC藥物,由人源化帕妥珠單抗的IgG1單抗、拓撲異構酶I抑制劑和酶促裂解四肽連接子(GGFG)組成,採用的偶聯方式是半胱氨酸殘基的定點偶聯,DAR爲8。適應症主要是EGFR突變的非小細胞肺癌、結直腸癌和乳腺癌。公司在2020 ESMO 會議上報道,根據I期臨牀試驗數據表明,U3-1402在49例經EGFR TKI和鉑類化療後進展的非小細胞肺癌患者中表現出抗腫瘤活性和安全性,整體ORR爲25%,爲耐藥患者提供新的治療選擇。
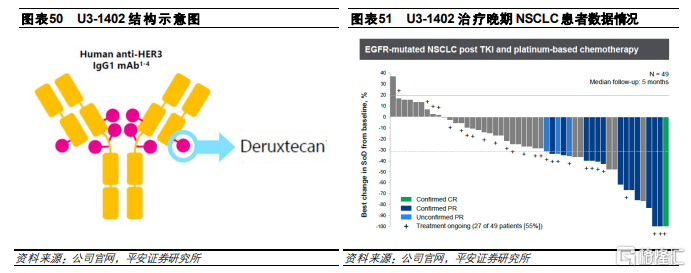
4.3 Seagen
Seagen成立於1998年,總部位於西雅圖,於2001年在納斯達克上市。公司是專家門診就ADC藥物開發的領先企業之一,開發出全球首個上市的二代ADC藥物Adcetris。隨後在2019年,公司開發的首個三代ADC藥物之一的Padcev也獲得FDA批準上市,進一步增厚公司業績表現。目前公司管線中共有7個ADC藥物,並與GeneTech、Abbvie、Astellas、Bayer、GSK與Genmab合作,或授權或合作開發了14款ADC藥物。
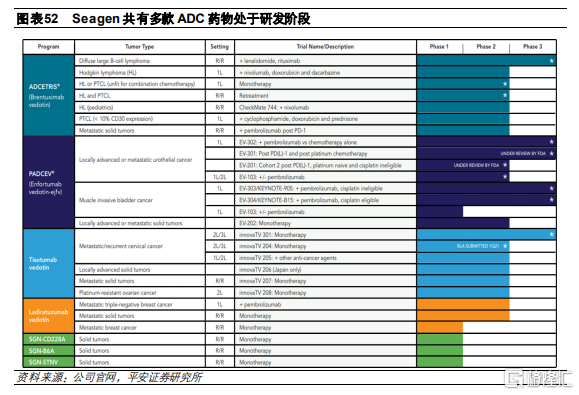
公司擁有ADC技術和糖工程技術平臺,其中糖工程技術能夠進一步增強抗體的ADCC效應,提高腫瘤殺傷效果,而ADC平臺中,公司在毒素、連接物、抗體、抗體改造技術研發及新靶點上均開展了創新嘗試:
在毒素上,公司嘗試多種新auristatin及其他類別的藥物;
在連接物上,公司的方向爲開發在血中更穩定在細胞中釋放毒素更有效的系統;
在抗體開發及新靶點嘗試上,公司開發針對新靶點的藥物並從學術團體及生物醫藥公司引進技術目前正與Agensys及OxfordBiotherapeutics合作;
在抗體修飾技術研究方面,公司進行抗體人源化、抗體去巖藻糖基化(增強ADCC)及改變抗體連接linker的位點的類型及數目(THIOMAB),能夠改善偶聯ADC時的效率及繁瑣程度。
Adcetris
Adcetris是一款靶向CD30的ADC藥物,由靶向CD30的嵌合IgG1抗體本妥昔單抗、微管抑制劑MMAE和可由蛋白酶剪切的二肽連接子組成,採用的偶聯方式是隨機偶聯,平均DAR爲4,分子量爲153kDa。
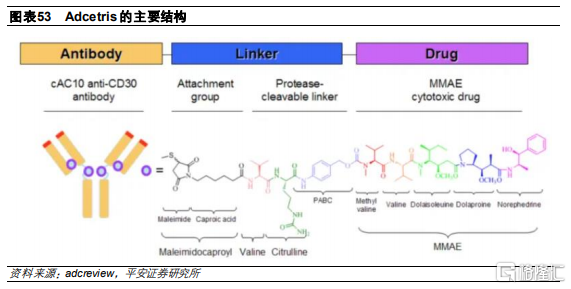
目前臨牀數據展現出Adcetris較好的治療潛力:
在一項涉及102例霍奇金淋巴瘤患者的臨牀試驗中,臨牀試驗結果表明,73%患者達到或完全或部分緩解,這些患者平均時間達到6.7個月;
在一項涉及58例全身間變性大細胞淋巴瘤患者的臨牀試驗中,臨牀試驗結果表明,86%患者達到或完全或部分緩解,這些患者平均緩解時間達到12.6個月;
在一項III期臨牀試驗中,共招募131名已經接受過治療的CD30陽性皮膚T細胞淋巴瘤(CTCL患者),試驗結果表明,接受Adcetris治療的患者中客觀緩解持續超過4個月的比率爲56.3%,顯著超過對照組的12.5%。
Padcev
Padcev是一款靶向Nectin-4的ADC藥物,由Nectin-4抗體AGS-22C3、微管抑制劑MMAE和可由蛋白酶剪切的二肽連接子組成,採用的偶聯方式是半胱氨酸殘基定點偶聯,平均DAR爲3.8,分子量爲152kDa。
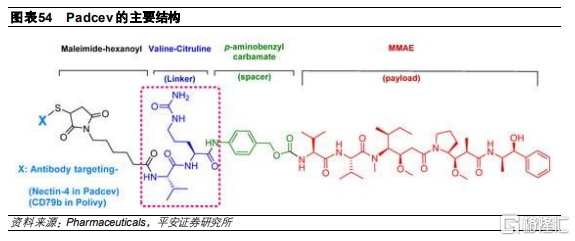
局部晚期或轉移性尿路上皮癌(EV-201)
這是一項II期、關鍵性臨牀試驗,隊列1入組曾接受PD-1/L1抑制劑治療和含鉑化療的患者共125名,隊列2入組未接受鉑類化療且不符合順鉑治療條件的患者共91名,所有患者接受1.25mg/kg的Padcev治療。臨牀結果顯示,隊列1和隊列2患者的ORR分別達到52%和44%,平均緩解時間分別達到10.9和7.6個月,展現出作爲後PD-1時代治療藥物的潛力。
聯合PD-1(Keyturuda)一線治療轉移性UC(EV-103)
這是一項Ib/II期、開發臨牀試驗,共入組45名局部晚期或轉移性尿路上皮癌患者,接受Keytruda和Padcev的聯合治療。結果顯示,患者ORR達到73.3%,CR達到15.6%,mPFS爲12.3個月。此外,組合療法組中83.9%的患者緩解持續時間超過半年,有53.7%的緩解的持續時間超過了1年。爲尿路上皮癌患者帶來無需化療的新治療選擇。
毒素爲MMAE的ADC和PD-1藥物具有協同效應。MMAE主要幹擾微管蛋白,會導致內質網應激和免疫原性細胞死亡。而免疫原性細胞死亡會進一步導致免疫激活分子的釋放,例如DAMP、毒素爲MMAE的ADC和PD-1藥物具有協同效應。MMAE主要幹擾微管蛋白,會導致內質網應激和免疫原性細胞死亡。而免疫原性細胞死亡會進一步導致免疫激活分子的釋放,例如DAMP、HMDB1等,從而激活天然免疫細胞殺傷腫瘤。而免疫抑制劑可以使免疫細胞能夠更好的識別並清除腫瘤細胞,產生協同效應。
4.4 榮昌生物
榮昌生物是一家創新生物製藥企業,成立於2008年,公司專注於ADC、抗體融合蛋白、單抗及雙抗等治療性抗體藥物領域。公司目前已開發了10餘款候選生物藥產品處於商業化、臨牀研究或IND準備階段,其中4款產品處於臨牀試驗階段,2產品進入商業化階段,分別爲泰他西普和維迪西妥。維迪西妥單抗(RC48)是我國自主研發並且首個獲得FDA授予突破性療法認定的國產ADC產品,於2021年6月在中國獲附條件批準上市。
維迪西妥單抗(RC48)
維迪西妥單抗(RC48)是公司自主研發的HER2-ADC產品,由靶向 HER2的人源化 IgG1單克隆抗體、可裂解多肽Mc-VC-PAB連接子和微管抑制劑MMAE組合而成,偶聯方式爲半胱氨酸隨機偶聯,平均DAR爲4。維迪西妥單抗雖然與Kadcyla均靶向HER2靶點,但具體靶向的HER2受體上的表位存在不同,具有更強的親和力和內吞性。
目前維迪西妥用於治療包括胃癌、尿路上皮癌、乳腺癌等多種實體瘤處於商業化或臨牀試驗階段,並已經初步展現出較好的療效,進一步驗證公司的ADC技術平臺能力。憑藉較好的臨牀療效,維迪西妥目前已經獲得藥監局兩項突破性療法認定和優先審評資格,以及FDA批準的快速通道資格和突破性療法認定,具有較大潛力。
多種HER2過表達實體瘤(I期)
這是一項I期、開放標籤、劑量遞增的臨牀試驗,數據顯示,在接受過該項試驗治療且數據可供分析的患者累計57名(包括47名胃癌患者及4名尿路上皮癌患者)中,患者的ORR爲17.5%,DCR爲49.1%。在胃癌患者的亞組分析中,2.0mg/kg和2.5mg/kg治療組的ORR分別爲20.7%和18.2%。在尿路上皮癌患者的亞組分析中,ORR爲50%,展現出較好的抗腫瘤活性。在此基礎上,公司進一步開展了維迪西妥單抗在胃癌及尿路上皮癌的II期臨牀研究。
HER2過表達胃癌(II期)
這是一項開放、單臂II期註冊性臨牀試驗,共招募了127名曾接受過至少兩次化療治療的 HER2過表達胃癌或胃食管結合部腺癌患者,接受2.5mg/kg Q2W維迪西妥單抗治療。臨牀數據顯示,患者ORR爲24.4%,mPFS爲4.1個月,mOS爲7.6個,延長患者生存期。憑藉該臨牀試驗數據,維迪西妥單抗於2021年6月獲得國家藥監局附條件批準上市,用於接受過至少兩種系統化療的HER2過表達(IHC2+或IHC3+)局部晚期或轉移性胃癌(包括胃食管結合部腺癌)患者的治療。
尿路上皮癌(II期)
這是一項開放、單臂的II期臨牀試驗,共招募43名曾經接受過全身化療的HER2過表達轉移性或不可切除尿路上皮癌患者,其中,32.6%的患者曾接受過至少兩種化療,20.9%曾接受過免疫治療。患者每2周接受1次2mg/kg劑量的維迪西妥單藥治療。臨牀數據顯示,患者ORR爲51.2%,DCR爲90.7%,mPFS爲6.9個月,mOS爲13.9個月。其中,有肝轉移的患者的ORR達到65%。
根據此項臨牀數據,公司開展了第二線單臂II期註冊性臨牀試驗,此臨牀試驗共招募64名曾經接受過全身化療(包括鉑類、吉西他濱、紫杉類)的HER2過表達局部晚期轉移性或不可切除的尿路上皮癌患者,接受維迪西妥2mg/kg Q2W的單藥治療。臨牀數據顯示,患者ORR爲50.0%,DCR爲76.6%,其中,對於IHC3+或IHC2+/FISH+的25例患者,ORR爲64%;對於既往僅接受過一線化療的9例患者,ORR爲55.6%;對於既往接受過2線化療的42例患者,ORR爲54.8%。所有患者的mPFS爲5.1個月,mOS爲14.2個月。
聯合特瑞普利單抗治療局部晚期或轉移性尿路上皮癌(Ib/II)
試驗共入組19例不限制 HER2表達狀態、 無法耐受或拒絕一線含鉑化療的局部晚期轉移性或不可切除的尿路上皮癌患者,接受維迪西妥1.5mg/kg+特瑞普利 3mg/kg、維迪西妥 2.0mg/kg+特瑞普利 3mg/kg治療方案。臨牀數據顯示,患者ORR達到94.1%,其中CR達到17.6%。
乳腺癌(I、Ib期)
I、Ib期臨牀試驗分別招募了70名HER2陽性乳腺癌患者和48名HER2低表達乳腺癌患者,其中,大部分(90.7%)患者發生過內臟轉移 ,70名HER2陽性患者中,70.0%曾接受過曲妥珠單抗等抗 HER2治療,48名 HER2低表達患者中,80.4%曾接受過內分泌治療。在70例HER2陽性患者中,接受1.5mg/kg、2.0mg/kg及2.5mg/kg劑量的患者亞組,ORR分別達到22.2%、42.9%和40%,mPFS分別爲4.0個月、5.7個月及6.3個月。在HER2低表達患者中也看到了較好的應答。
4.5 樂普生物
樂普生物是一家聚焦於腫瘤治療領域的創新型生物製藥企業,成立於2018年。公司的生物藥研發能力包括三個針對不同生物療法的專門平臺,包括ADC技術平臺、抗體發現平臺、具備先進工藝的分析開發平臺。公司的ADC平臺使用的偶聯技術是從Synaffix引進的GlycoConnect™(酶重塑定點偶聯),主要是利用天然糖基化位點實現定點偶聯,用於構建新一代ADC藥物。憑藉豐富的技術平臺,公司目前共擁有8款進入臨牀階段的候選藥物,其中包括5款ADC療法、2款免疫節點藥物和1款溶瘤病毒,是目前國內擁有較豐富ADC管線的領軍企業之一。
MRG003
MRG003是公司自主研發的EGFR-ADC產品,由抗EGFR的IgG1單克隆抗體、可裂解肽鍵vc-PABC連接子和微管抑制劑MMAE組合而成。公司使用的EGFR單抗相比西妥昔單抗的結合親和力提高約6-7倍,具有更好的內吞性。
這是一項開放標籤的I期臨牀試驗,Ia期共招募22名晚期HNSCC、NPC及CRC患者,Ib期共招募39名EGFR表達陽性的HNSCC、NPC及CRC患者。從臨牀結果來看,Ia期未檢測EGFR表達情況的患者中,整體ORR僅爲5.6%,DCR爲33.3%。而在Ib期EGFR表達陽性的患者中,整體ORR達到30.3%,DCR爲63.0%,其中,HNSCC、NPC和CRC患者的ORR分別爲40.0%、44.0%和25.0%。
MRG002
MRG002是公司自主研發的HER2-ADC產品,由嵌合利妥昔單抗、可裂解肽鍵vc-PABC連接子和微管抑制劑MMAE組合而成。公司使用的改良版曲妥珠單抗相比曲妥珠單抗在Fc區域具有選擇性的較高巖藻糖基化水平,進一步降低了抗體對於CD16a免疫細胞的潛在殺傷性,減少患者不良反應。
HER2陽性實體瘤
這是一項開放標籤的I期臨牀試驗,Ia期共招募25名晚期HER2陽性實體瘤患者。臨牀結果顯示,在21名可評估療效的患者中,整體ORR達到42.9%,DCR爲81.0%。其中,16名HER2陽性乳腺癌患者亞組中,ORR達到50.0%,DCR達到81.3%。
MRG001
MRG001是公司自主研發的CD20-ADC產品,由利妥昔單抗生物類似藥、可裂解肽鍵vc-PABC連接子和微管抑制劑MMAE組合而成。
HER2陽性實體瘤這是一項開放性I期臨牀試驗,共招募18名CD20陽性B細胞非霍奇金淋巴瘤患者。目前,一名FL患者在0.15mg/kg劑量下達到PR,一名DLBCL患者在1.8mg/kg劑量下達到CR,一名FL患者在2.5mg/kg劑量下達到PR。
05
投資建議
5.1 關注有臨牀價值和差異化的高壁壘創新賽道
同質化創新藥陷入價格和速度比拼。從我國創新藥研發階段來看,過去爲了快速跟進國外成熟藥物的me-too類創新賽道已經較爲擁擠,藥物研發的同質性問題顯著,導致新藥上市可能就將面臨集採,例如PD-1單抗藥物,最終仍然落入價格、銷售能力和推進速度的比拼。
我國創新步入2.0時代。伴隨研發能力提升,目前我國部分企業的研發正在逐步從創新1.0轉型到2.0階段,演變成me-better/faster的差異化競爭,逐漸與國際接軌,填補尚未滿足的適應症空白。在這個階段,獲得國際認可的創新藥企有望走出國門,產品實現全球化銷售,海外市場相比醫保市場具有更高議價能力,提升企業盈利能力。因此,在創新2.0時代我們需要關注具有較高壁壘的研發賽道,這個研發壁壘主要體現在技術和靶點方面:
高壁壘創新技術平臺。佈局技術壁壘相對較高的前沿領域的企業。這類賽道護城河較寬,前期平臺研發需要較多積累,領軍企業先發優勢顯著,此外,自主技術平臺能夠賦能管線研發,企業具有持續造血能力。
尚未驗證的創新靶點。佈局開發難度較大的創新靶點的企業。這類靶點有望革新治療方式,有望創造較高臨牀價值,市場潛力較大且尚未形成明顯競爭格局,例如CD47、CD73、SHP2等。
ADC就是高壁壘創新賽道之一,擁有較深護城河以及較大發展潛力。隨着ADC技術的不斷迭代和成熟,ADC藥物治療效果和作用力持續提升,目前已在臨牀試驗中取得優異的療效,展現出其在後線治療中的優勢,填補仍然空白的適應症,同時有望推進前線,取代部分現有療法,具有較大市場潛力。此外,目前仍有較多ADC藥物處在臨牀階段,伴隨藥物研發推進,未來幾年ADC行業即將迎來收穫期,步入全面商業化時代,市場容量將持續擴大。
5.2 ADC賽道中關注有自主平臺以及進度較快的企業
平臺是企業持續造血的關鍵。ADC作爲人爲組合藥物,每一個組成部分都可以變化替換,具有豐富的可能性。但在構建過程中也存在較多需要解決的問題,包括均質性、穩定性以及安全性等,技術平臺價值凸顯。具備自主技術平臺的企業有望能夠組合迭代不同產品,賦能產品管線研發,同時有望通過轉讓項目增厚業績,具有一定稀缺屬性,建議關注這類具有高壁壘技術平臺的研發型企業。
進度靠前的企業具備先發優勢。由於我國ADC行業正在逐步從fast-follow轉型,因此目前處於臨牀後期階段的產品存在同質性。參考PD-1單抗競爭情況,研發進度較爲靠前或者適應症差異化佈局的企業有望能夠在上市後迅速佈局市場,具備顯著先發優勢,建議關注成熟靶點中處於第一梯隊的企業和產品。
差異化產品有望開拓全球市場。我國ADC行業正在初步追求差異化轉型,企業開始自行探索競爭格局尚未明確、全球還沒有成熟產品的靶點和方向,或者構建在同靶點中功能更優的ADC分子,有望進一步提高ADC藥物療效以及擴大使用範圍,走向全球市場,建議關注靶點或分子具備差異化的產品和企業。
CRO企業有望能夠受益於研發熱潮。ADC藥物開發門檻較高,而我國多數藥企過去只具備做仿製藥的能力,在自主創新方面能力仍然有待提高。部分傳統企業爲了轉型附加值更高的創新藥賽道,佈局ADC領域,將和具備研發能力的CRO企業合作,利好其業績表現。
06
風險提示
6.1 研發風險
ADC產品目前基本仍然研發階段,新藥研發受到資金、政策、技術等多因素影響,存在進度不及預期甚至失敗的可能。
6.2銷售風險
部分ADC研發企業現在尚無產品商業化經驗,銷售團隊能力還沒有得到驗證,未來藥物上市後可能存在推廣不及預期的風險。
6.3競爭加劇風險
未來可能會有更多企業佈局ADC領域,導致競爭局面惡化。
6.4政策風險
作爲新興技術,行業監管政策存在發生變動的風險。



