疫苗,被列入20世紀10項最偉大的公共衞生成就之一,能夠有效控制疾病傳播,節約高額醫療衞生支出。根據WHO數據顯示,截止2018年底,全球共批准針對41種疾病的77種預防性疫苗,覆蓋約2/3的重要疾病。但現階段,仍有超過20種疾病因缺少針對性疫苗,未能得到有效預防和控制。
那麼,在後疫情時代下,未來疫苗行業發展趨勢如何,投資價值在哪裏?格隆匯有幸採訪了疫苗行業的佼佼者成大生物相關人員,分享有關疫苗行業的看法與觀點。以下為內容摘要:
疫苗行業:多聯多價苗受青睞
根據中信證券數據顯示,2020年,中國已經成為全球第二大疫苗市場,銷售收入佔全球市場的15.5%。伴隨着龐大的人口基數、民眾日益增強的防疫意識以及二類苗需求增加,我國整體增速遠高於全球疫苗市場增速,上升空間大。
Q1:相較於其他產品,疫苗的生產和運輸方面是否存在特別的要求?
A1:疫苗生產企業首先要取得藥品生產許可證,生產全過程需要符合新版藥品GMP要求,運輸需要符合《疫苗儲存和運輸管理規範》要求,切實保障疫苗全程2-8℃精準温控,達到全程冷鏈和全程可追溯的管控要求。
Q2:疫苗行業的未來發展趨勢如何,是否有特別看好的疫苗品種?
A2:從已經公佈的2020年全球疫苗市場銷售情況來看,全球TOP10疫苗產品總銷售額達到217.9億美元(佔全球疫苗市場的62%),其中肺炎結合疫苗、HPV疫苗、B羣流腦疫苗、帶狀皰疹疫苗和聯合疫苗,以及其他應用mRNA等新技術研發的疫苗備受矚目。
圖表一:2020年全球TOP10疫苗產品
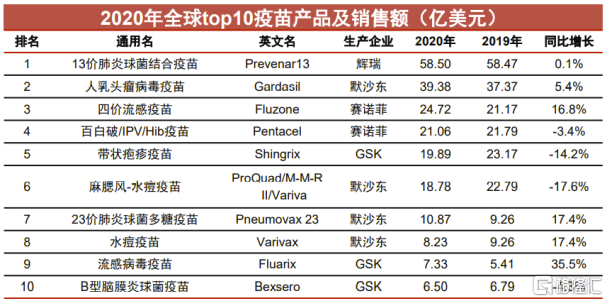
數據來源:中信證券,格隆彙整理
總體來看,世界疫苗的研發重點由單價疫苗轉向多價以及聯合疫苗。技術迭代是疫苗產業的發展趨勢,高價次疫苗會替代低價次疫苗,聯合疫苗會替代單苗,當然替代不會一蹴而就,需要產能供應保障和價格適當,還需經歷一定的時間週期,但潛在市場疊加將會帶來巨大的增量空間。
創新型疫苗:未來主流趨勢
伴隨着行業准入門檻和規範程度不斷提高,疫苗技術迭代升級發展,疫苗行業的整合重組大勢所趨,集中度也有望快速提升。一些規模小、品種單一、缺乏核心研發能力、生產水平落後的疫苗企業將面臨淘汰或者併購的生存壓力,而研發管線豐富並且具有領先創新研發實力的優勢疫苗企業未來將會佔領更多的市場份額。
Q3:在創新型疫苗中,四價流感病毒裂解疫苗市場空間如何?
A3:2018年6月,國內首個4價流感疫苗獲批上市,截至目前,華蘭生物、江蘇金迪克、科興生物和長春所等6家企業的4價流感疫苗已經獲批上市。整體來看,流感疫苗市場潛力較大,歐美髮達國家的流感疫苗接種率在20%—30%之間,國內的接種率不到4%,如果未來提升到8%,則對應1億劑左右的流感疫苗市場規模,未來增量空間值得期待。
其中,成大生物的四價流感疫苗通過採用WHO推薦的流行毒株,經過雞胚孵化培養收穫病毒,結合滅活疫苗生產工藝製備而成。採用均質技術製備,能有效防止抗原聚合,減少注射痛和過敏等副反應的發生。產品上市之後將面向國內和國際兩個市場,快速實現商業化。
Q4:手足口病近年來也是一個市場重點關注的疾病。據悉,手足口病疫苗2016年已獲批上市,為何僅在中國接種?
A4:手足口病疫苗是我國自主研發的創新疫苗,2016年昆明所的二倍體手足口疫苗率先上市,接着科興生物和武漢所的手足口疫苗也先後上市。EV71病毒導致的手足口病在全球都有流行,其中我國大陸地區疫情特別嚴重,疾病防控負擔大。截至目前,境外尚無手足口疫苗上市,國產手足口疫苗也未在境外獲批出口註冊,所以僅在中國接種。
Q5:B羣流腦疫苗目前有輝瑞公司的Trumenba以及葛蘭素史克公司的Bexsero,這款疫苗在國產替代的空間大不大?
A5: 葛蘭素史克公司的B羣流腦疫苗(Bexsero)2020年的全球銷售額約7億美元,是全球排名前10的重磅疫苗品種。
我國B羣流腦的發病率逐年上升並且中國目前尚無針對B羣流腦的疫苗上市,成大生物研發的B羣流腦疫苗能夠對B羣流腦的發病起到預防作用,使用專門構建的生產株進行製備,不僅降低了脂多糖毒性,還保持了脂多糖的佐劑作用,增加了疫苗生產量和有效性。上市之後將填補國內空白,面臨廣闊的市場空間。
成大生物:不止於狂犬疫苗的“一哥”
頂着“狂犬疫苗一哥”的光環,成大生物10月成功登陸科創板。然而,成大生物在疫苗領域的佈局,並不止於此,其產品管線之豐富,爆發之時指日可待。
Q6: 根據公司招股書披露,當前公司佈局了24個在研項目,其中不乏許多新品類疫苗的開發,比如四價流感病毒裂解疫苗、A羣C羣腦膜炎球菌多糖結合疫苗、15價HPV疫苗等,請問公司這樣佈局候選疫苗的出發點是什麼?
A6:總體來看,公司佈局候選疫苗的出發點有3個:
(1)承擔保障疫苗供應的社會責任。公司積極響應國家關於疫苗產業的發展規劃和支持政策等戰略要求,保證重點疫苗的品種和產能能夠滿足國家需求。
(2)有效支撐公司發展戰略,豐富公司產品線以適應公司未來戰略發展需要。在疫苗研發方面,公司構建了病毒性疫苗、細菌性疫苗、重組蛋白疫苗和多聯多價疫苗等技術研發平台,同時與全球知名的學術機構和企業進行合作研發,通過技術合作的方式側重研發重磅創新品種。
(3)綜合評估疫苗品種的研發可行性與商業化價值。基於各大技術平台,公司專注於發展具有較大市場潛力的傳統疫苗的升級換代和創新疫苗的研發,並圍繞國家疫苗供應體系規劃積極推進多聯多價疫苗的開發,佈局並加速20餘個在研疫苗項目的研發進程。
目前,公司16個在研項目處於臨牀前研究階段,2個在研項目已取得臨牀批件,4個在研項目進入臨牀I期,1個在研項目進入臨牀III期。其中,13價肺炎球菌結合疫苗、甲型肝炎滅活疫苗、b型流感嗜血桿菌結合疫苗、A羣C羣腦膜炎球菌多糖結合疫苗、四價雞胚流感病毒裂解疫苗、凍幹人用狂犬病疫苗(人二倍體細胞)和狂犬疫苗四針法工藝研究已取得臨牀批件。
Q7:公司的在研管線中,佈局了很多的創新疫苗,為何會選擇創新疫苗進行研發?
A7:按照新版《藥品註冊管理辦法》,疫苗可分為創新型疫苗、改良型疫苗和境內外已上市疫苗。相對而言,創新型的新品種疫苗進入壁壘較高,研發週期較長,註冊上市的審批要求更加嚴格。
新版《藥品註冊管理辦法》的出台,為創新疫苗的加速審批上市提供了有力的政策支持,同時創新疫苗具有較高的技術壁壘和較長的專利週期,能給企業帶來豐厚的投資回報。因此,以研發創新驅動企業發展成為公司的發展戰略。
在疫苗創新研發方面,公司構建了病毒性疫苗、細菌性疫苗、重組蛋白疫苗和多聯多價疫苗等技術研發平台,並加速推進20價肺炎疫苗、15價HPV疫苗和B羣流腦疫苗等創新品種的研發進程,同時公司將密切關注全球疫苗發展動態和市場需求,保持對疫苗領域新產品、新技術的敏感性,不斷提升研發創新能力和項目成功率。
Q8: 具體來看,公司在創新疫苗的開發方面,從研發到商業化階段做了哪些準備?
A8:公司在創新疫苗開發上,主要從以下三方面做準備:
(1)建立獨立自主的研發平台。目前,公司已建立獨立且體系完整的研發平台,能夠獨立開展研發活動,其中包括細菌疫苗技術平台、病毒疫苗技術平台和多聯多價疫苗技術平台的建設。基於該等獨立的研發平台,公司擁有多種自主開發的疫苗產品。
圖表二:成大生物獨立研發平台

數據來源:公司招股書,格隆彙整理
(2)自主研發+合作共贏模式雙輪驅動。一方面,公司堅持核心技術的自主研發,另一方面,公司積極與全球知名的學術機構和企業進行合作研發,通過技術合作的方式側重研發重磅創新品種。公司建立了一整套合作機構篩選、評價和管控的機制,保證了高效的創新項目合作。
(3)創新疫苗商業化能力強。公司擁有領先的生產能力和豐富的產業化經驗,先後建成瀋陽和本溪兩個疫苗生產基地,確保創新疫苗品種獲得上市註冊批准之後,能快速實現產業化。公司擁有自營團隊為主體的國內銷售團隊和網絡覆蓋一帶一路30多個國家的國際銷售團隊,產品上市之後將面向國內和國際兩個市場,快速實現商業化。
Q9:當下,九價HPV疫苗一苗難求,部分地區甚至出現比搖車牌的中籤率還低。目前國產高階HPV疫苗競爭格局如何?在研發中可能存在哪些困難需要克服?
A9:2020年,國內HPV疫苗的批簽發數量約1300萬支,市場規模約為140億元左右(按批簽發量*中標價格估算),市場規模呈現快速增長態勢。2017年,史克和默沙東的HPV疫苗先後在國內獲批上市,2020年默沙東的4價和9價的批簽發量合計約為1200萬支,銷售額大約為130億元,呈現穩步上升態勢。史 克的2價批簽發量為69萬支,銷售額約為5.5億元,呈現逐年下降趨勢;萬泰生物的2價HPV在2020年上市,批簽發量為246萬支,銷售額約為8億元。
圖表三:HPV疫苗批簽發情況
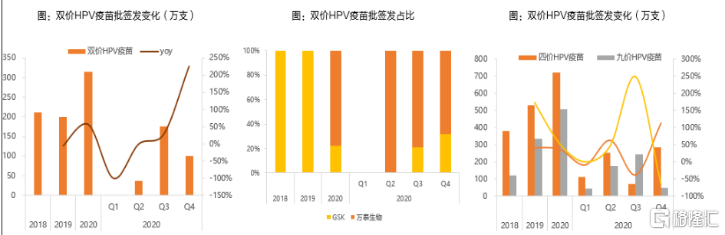
數據來源:天風證券,格隆彙整理
在研發方面, HPV疫苗是基於重組HPV的L1蛋白形成的病毒樣顆粒(VLP)技術,只有與天然病毒一樣結構的VLP方可產生良好的免疫原性。VLP正確結構的形成不僅基於基因序列的正確,培養條件和細胞內微環境也至關重要,因此VLP的表達量和維持以及優化其結構正確性的純化工藝是生產HPV疫苗的技術門檻和主要挑戰。
Q10:關注到成大生物佈局15價HPV疫苗。一般來説,越高價的疫苗越難研發。那麼成大生物為何不從低價的疫苗快速切入,而是首次就選擇了高價的HPV疫苗?
A10:公司採取自主研發為主,合作研發為輔助的研發模式。2019年,公司和康樂衞士簽訂《15價HPV產業化技術開發合同》,雙方合作研發15價HPV疫苗。康樂衞士在HPV疫苗研發方面起步較早,具備HPV疫苗開發技術和經驗,該公司的3價和9價HPV已經進入臨牀III期階段,合作方具備成熟的臨牀前研究經驗,公司與其合作,可以節約大量工藝摸索的時間。成大生物合作研發的15價HPV疫苗,能夠覆蓋全部高危型HPV,並獨立進行生產和銷售,上市之後將對9價HPV形成替代優勢。
Q11: 今年6月8日輝瑞全球首款的20價肺炎球菌結合疫苗獲美國FDA批准上市, 20價肺炎球菌結合疫苗的未來前景如何?成大生物在國內處在第幾梯隊?
A11: 根據國家統計局的數據,2020年我國出生人口數量1200萬人,近年國家大力鼓勵三胎政策,預計到2029年出生人口數量將不會低於1200萬人。按照50%的接種率估算,每人均完成4針的接種程序,則肺炎結合疫苗的潛在市場需求為2400萬支。基於國家人口普查數據,2020年,大陸地區60歲及以上的老年人口總量為2.64億人,已佔到總人口的18.7%。大致預測到2029年,60歲以上人羣數量為3億人。接種肺炎疫苗(23價多糖和20價結合)的人羣佔比為50%,接種程序為1劑(超過5年再次接種),則老年人每年的市場規模約為3千萬劑。
20價肺炎結合疫苗上市之後,將會分別替代兒童市場的13價肺炎結合和老年人市場的23價多糖疫苗,規模合計約2200萬支,按照800元/支計算,對應市場規模約為176億元。在兒童市場,高價次的20價肺炎將逐步取代低價次的13價肺炎,假設20價肺炎佔據50%的市場份額,則為1200萬支,兒童市場規模約為96億元;在老年人市場,逐漸替代23價肺炎疫苗,佔據1/3市場的老年人市場,則市場規模為1千萬支,對應銷售額約80億元。
2021年6月,20價肺炎球菌結合疫苗的成人適應症在美國獲批,當前,國內目前還沒有20價肺炎球菌結合疫苗上市。
近期輝瑞將開始在我國做進口註冊的臨牀試驗,主要用於兒童。國內的萬泰生物和成大生物在20價肺炎疫苗研發方面進展較快。2021年9月,萬泰生物與江蘇坤力聯合開發的20價肺炎疫苗獲得臨牀批件。
成大生物自主研發的20價肺炎疫苗在2017年5月正式立項,目前處於臨牀前研究階段,預計未來幾年推進至上市階段,研發進度在國內處在第一梯隊。



