近期,国家药品监督管理局药品审评中心(CDE)发布一则“关于公开征求《以临床价值为导向的抗肿瘤药物临床研发指导原则》意见的通知”。
在药物进行临床对照试验时,应尽量为受试者提供临床实践中最佳治疗方式/药物,而不应为提高临床试验成功率和试验效率,选择安全有效性不确定,或已被更优的药物所替代的治疗手段。
新药研发应以为患者提供更优的治疗选择为最高目标,当选择非最优的治疗作为对照时,即使临床试验达到预设研究目标,也无法说明试验药物可满足临床中患者的实际需要,或无法证明该药物对患者的价值。
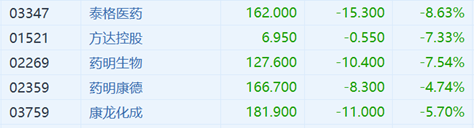
受消息面的影响,7月6日开盘,港A市场CRO概念股全线下跌。截至发稿,A股泰格医药大跌近11%,美迪西跌超10%,而10日内跌近30%;泰格医药跌超7%,药明康德跌超4%;港股泰格医药大跌8.6%,药明生物、方达控股大跌超7%,康龙化成跌近6%,药明康德跌近5%。
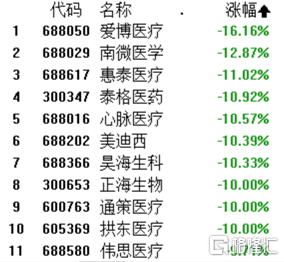
这个趋势也从CRO板块蔓延到了整个医药板块,港A市场医药板块迎来黑天鹅,正海生物、通策医疗、拱东医疗跌停,艾博医疗暴跌16%,心脉医疗、慧康医疗、昊海生科、跌超10%。伟思医疗触及跌停,大热的“眼科茅”爱尔眼科暴跌超7%,医美巨头爱美客重挫近7%。
如此看来,这波由CRO概念股带起闪崩,极大的影响了整个医药行业,疯涨的医药行业泡沫要被戳破了吗?
1
中国医药的至暗时刻
十七年前,中国医药产业迎来了“疯狂”的一幕,仅2004年一年内,国家药监局受理了包含仿制药的10009种“新药”的申请,而太平洋彼岸的美国仅受理了148种。
而这种疯狂伴随的是,医药审批成为了“明码标价的商品”,药品临床试验数据多数造假,大量劣质甚至无效药进入市场,再经过经销商层层加价、医院吃满回扣后,流入百姓的手中。
此次爆发之后,2005年开始中国医药行业自此进入了几近停滞的十年寒冬,2013年药品审评中心批准上市的药品,仅有416个。医药审批也从04年的“大跃进”骤然转入“停滞不前”的境地。
截至2015年,一共积压了2.1万件药品审批,其中仿制药占80%。有药品研发机构的负责人称,“以目前的审批速度,中国患者要吃上已经研发好的药,光拿批文号就要等16年。”
时任国家食品药品监督管理总局副局长吴浈称,“很多企业在资料还不完整的情况下就申报,甚至还有作假的情况,对这样的药品,监管不敢批。”

而在这个时刻,出现了一个打破“没有创新药、看不到未来”的医药行业的标志性事件,后来也被称为是医药行业“七二二惨案”。
2015年7月22日,国家食药监局发布《关于开展药物临床试验数据自查核查工作的公吿》,要求申请上市的1622个药品注册申请的企业自查,数据不真实的要主动撤回,821家药企面临割肉抉择。如果发现数据造假,不仅要立案调查,并且三年内再度申请的药品不予受理。
这一次,药品造假者自己种下的苦果也只能硬生生的往肚子里咽了,同济医院、协和医院等大三甲医院也没有幸免,最终1622个药品注册申请中,撤回了85.5%。
在此事件之后,同年8月,国务院印发《关于改革药品医疗器械审评审批制度的意见》,被称为是中国创新药史上最重要的“44号文”,重新定义了新药和仿制药,提高了把审评门槛。
此前,不论在境外是否上市,只要未在中国境内上市的都叫做新药,修改后,标准和美国FDA一致:此前境内外都未上市的药,才能称为新药。
而仿制药的判定也从仿制有国家标准的药,直接提高为“原研药”。大部分混入“新药”的药品,瞬间失去了专利期的保护伞,堕入了仿制药行业。而和国外接轨的“新药”在审批上将一路绿灯。
多少年后再度回望,“722惨案”也许可以成为制药史上一座具有意义的里程碑,会有很多人都会感谢这次的核查。
但新的问题也在悄然生长。
2
“Me-too”时代已经终结
近年来,在贪婪血腥资本的助推下,创新药行业乱象丛生,很多“创新”药企不去发现更加优秀的药物分子,而是扛上“创新药”的大旗,对已经上市的创新药寻求小修小改,再套上一个个绚丽的故事。
其中肿瘤相关药物的问题尤为严重,根据国家6月21日发布的年度药品审评报吿显示,2020年CDE批准了650项抗肿瘤药物临床试验申请项目,其中化学药355项,生物药294项。而这些IND申请,大部分的项目要么是讲故事,要么是直接销声匿迹。
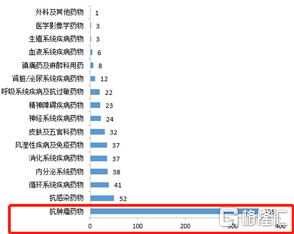
(2020年1类创新化学药IND申请情况)
而《指导原则》的发布,被视作是对目前严重研发“内卷”肿瘤药物的一记重拳,目前有很多Biotech(生物科技)靠着有套利需求的资本催化,与CRO(医药研发外包)企业合作购买研发管线,最后抱团上市套利。
而生物科技研究团队、资本与CRO企业互相画饼,侵占了本已有限的临床资源,浪费大量资金以催生出批量的“Me-too”创新药研发项目,创造出一个个资本神话和“新药”传奇。而一大批CXO(医药外包服务)企业涌现,行业也空前繁荣,市场中也出现药明康德、泰格医药、康龙化成和凯莱英等一批CXO(CRO、CDMO)大牛股,形成所谓的“黄金赛道”。
这些“Me-too”药物,避开“专利”药物的产权保护的新药研究,以现有的药物为先导物进行研究,进行分子结构改造或修饰。但为了圈钱一味盲目上市的“Me-too”药物,无疑是搅乱创新药的研发。
这么看来,政策的发布是对进行Me-too类药物研发的企业提出了更高的要求,过去鱼目混珠的Me-too时代已经过去离去。而作为它们下游研发外包服务商的CRO行业可能面对订单数量骤减等情况,迎来结构的分化。
3
看似是尖刀?实则是双刃剑
受消息面上的影响,昨日市场上就已有所反映,截至5日收盘,CXO、CRO相关股票大跌,泰格医药A股收跌超5%,H股收跌超3%;药明康德和康龙化成在上一个交易日双双暴跌之后,昨日依然以下跌收报;临床龙头股美迪西收跌6.07%,上周五大跌超13%,最大跌幅一度超过14%。
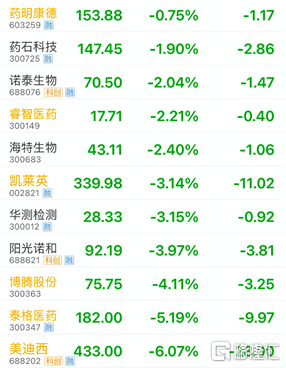
虽然市场反应剧烈,但是业内普遍认为,政策虽然打压了Me-too药品,但对创新药企业起到了极大的推动作用,有了这个指导原则,创新药的春天真的到来了。
业内人士表示,《指导原则》把药企人一直在想的、一直以为难以实现的很多方面,都表达了出来,而此次的原则也是延续了2015年以来,CDE一贯的政策改革趋势。
而政策的发布究其根本,并不是为了打压有创新药研制能力的医药龙头企业,而是解决当下市场乱象丛生的现状,让一些鱼目混珠的劣质药企知难而退,“马太效应”或将会进一步显现。
对于中国的医药行业来说,研制创新药还要不要?一定是要的!而且未来还会出现越来越多优质的Me-better和Me-new的创新药物。
那这么来看,对这些药物有效性的判断就必须经过临床试验后才能得出结论,而药物一旦进入了临床试验阶段,研发外包的订单就已经在CRO企业的手中了。
从中国临床试验CRO市场规模来看,从2016年的17亿美元上升至2020年44亿美元,年复合增长率为26.8%,预计2021年将进一步扩大至56亿美元,将呈快速增长趋势。
对于真正有能力的生物医药和研发创新药的企业来说,有优秀龙头CRO的加持,从临床(患者)需求的角度找准产品定位,拿着更加优秀的动物实验数据向监管层申请的临床试验的时候,有什么理由埋没优质的创新药呢?
4
总结
从整个医药生物板块来看,6月21日至7月4日内板块涨幅为2.76%,而年初至今,医药生物板块涨幅为10.71%,其中细分行业的医疗服务、中药和医疗器械分别大涨30.14%、25.85%和14.61%,可以说是绝对的大牛赛道。
因此在此次消息面的刺激下,前期涨幅太大、获利盘较多的CXO(CRO)产业在此时出现了整体的回撤,也是估值过高的合理回落。
从中长期来看,目前CRO行业保有较大的增量市场,投资者可以选择估值相对合理、基本面稳固的龙头企业。



